銅綠假單胞菌快速檢測方法的優化研究
2021-12-10 16:33:54 來源: 世界杯賽程預測 導刊
單 萌1,周 婀1,馬 瑜2*
(1.上海康識食品科技有限公司,上海 201101;
2.陝西省微生物研究所,陝西西安 710043)
摘 要:為優化銅綠假單胞菌檢測方法,本研究對不同選擇性培養基的篩選效力及選擇性進行了評價,並按照GB 8538—2016對人工汙染樣品進行了檢驗;進而,將選擇性培養基鑒定結果與VITEK 2 Compact全自動細菌鑒定係統和基質輔助激光解析電離飛行時間質譜技術(MALDI-TOF-MS)結合,對不同檢測技術、方法的有效性、適用性及相互之間的融合性進行了比較和分析,以期提升銅綠假單胞菌的檢測效率及準確度。結果表明,乙酰胺瓊脂上銅綠假單胞菌的特異性較差,會出現假陽性或假陰性結果;而銅綠假單胞菌顯色培養基(RAPID’s P.aeruginosa Agar)則具有典型的菌落特征以及較短的增菌時間,因此,將該培養基與VITEK 2 Compact係統結合使用可有效提高檢測的靈敏度、特異性及時效性,適用於對大批量樣品進行快速判定。
關鍵詞:銅綠假單胞菌;快速檢測方法;優化
Comparison and Optimization of the Rapid Detection Method for Pseudomonas Aeruginosa
SHAN Meng1, ZHOU E1, MA Yu2*
(1.MasterKong CO., Ltd., Beverage IRD Center,Shanghai 201101,China;2.Shaanxi Institute of Microbiology, Xi'an 710043, China)
Abstract: In order to optimize the detection method for Pseudomonas aeruginosa, comparison of the effectiveness and selectivity of different selective media was performed, and the artificially contaminated samples were tested according to the GB 8538—2016. Finally, for the purpose of improving the detection efficiency and accuracy of P.aeruginosa, the results obtained above were combined with the VITEK 2 Compact and MALDI-TOF MS Biotyper System. The effectiveness, applicability and integration of the three detection methods were compared and analyzed. The results showed that the specificity of acetamide agar for Pseudomonas aeruginosa was poor, and accompanied with false positive/negative results occasionally. However, the RAPID’s P.aeruginosa Agar was notable for its typical colony characteristics and short incubation time. Therefore, the combination of RAPID’s P.aeruginosa Agar with the technique of VITEK 2 Compact System was suitable for rapid determination of large quantities of samples with the , which can improve the sensitivity, specificity and timeliness of the detection remarkably.
Keywords: ; rapid detection method; optimization
銅綠假單胞菌(),屬假單胞菌屬,廣泛分布於水、土壤、空氣、植物、汙水、醫院、動物及人體內等各類環境中,是一種常見的水源性和食源性條件致病菌[1-3]。該菌可引起機體組織器官病變甚至壞死,進而引起腸胃炎、敗血症等病症及不同程度的人畜共患性傳染病;同時,其產生的多種致病因子容易引起免疫力低下及受抑製人群或長期使用抗生素人群的化膿性感染和耐藥性問題[4-5]。此外,銅綠假單胞菌形成生物膜後,對幹燥、紫外線、消毒劑等理化因素及不良環境具有較強的抵抗力;且由該菌汙染引起的產品腐敗會嚴重影響產品品質,導致經濟損失。因此,實現銅綠假單胞菌準確、快速檢測一直是食品加工業的關注重點和迫切需求[6]。
利用培養基對微生物菌群中特定微生物具有選擇性的這一特征,可以通過不同的選擇性培養基從環境中對微生物進行分離。而關於銅綠假單胞菌的檢測主要依賴於培養方法,其中最為關鍵的是選擇合適的培養基。目前,已有多種選擇性培養基,如抗生素篩選培養基[7]、色素篩選培養基[8]及乙酰胺培養基[9]可用於假單胞菌的分離篩選。我國關於銅綠假單胞菌的檢測大多依據GB 7918.4—1987[10]和
GB 8538—2016[11],此外,國標GB 19298—2014中明確規定各類抽檢水樣品中均不得檢出銅綠假單胞菌[12]。但上述標準中的檢測方法主要依賴於傳統的分離培養、形態學觀察及生化鑒定等檢測手段,檢測耗時長、過程煩瑣、且容易出現假陽性或假陰性結果,不利於企業快速判斷結果,進而造成檢測結果滯後。因此,實現銅綠假單胞菌的快速、準確檢測具有重要意義。
隨著人們生活水平和對健康意識的不斷提高,包裝飲用水成為了許多家庭和集體飲用水的首選。近年來,隨著包裝飲用水的消費數量的不斷上升、產品種類及包裝方式的多元化,包裝飲用水中檢出銅綠假單胞菌的報道逐漸增多,原有的傳統檢測方法已難以滿足當前的生產需求[13]。本研究同時對用於銅綠假單胞菌檢測的4種不同培養基的篩選效力及選擇性進行了評價,進而通過將選擇性培養基鑒定結果與VITEK 2 Compact全自動細菌鑒定係統和基質輔助激光解析電離飛行時間質譜技術(MALDI-TOF-MS)結合,對不同檢測技術、方法的有效性、適用性及相互之間的融合性進行了比較和分析,以期提升銅綠假單胞菌的檢測效率及準確度。
1 材料與方法
1.1 材料與儀器
標準菌株共 5 株, 包 括: 銅 綠 假 單 胞 菌(Pseudomonas aeruginosa)ATCC27853(N-1)、 大腸埃希氏菌(Escherichia coli)ATCC25922(N-2)、熒光假單胞菌(Pseudomonas fluorescens)ATCC13525(N-3)、 嗜 麥 芽 寡 養 單 胞 菌(Stenotrophomonasmaltrophilia)ATCC51331(N-4)、鞘氨醇單胞菌屬(Sphingobacterium)ATCC31555(N-5),為廣東微生物菌種保藏中心保藏菌種。其中,銅綠假單胞菌N-1 (P. aeruginosa)ATCC27853 作為陽性對照,其餘菌株為陰性對照。G-1(銅綠假單胞菌,P.aeruginosa)、G-2( 銅 綠 假 單 胞 菌,P.aeruginosa)、G-3( 銅 綠假單胞菌,P.aeruginosa)、G-4(惡臭假單胞菌,Pseudomonas putida)、G-5(少動鞘氨醇單胞菌,Sphingomonaspaucimobilis)為本實驗室保存菌株,乙酰胺實驗結果均呈陽性。其中,G-1、G-2、G-3 分離自水源水,G-4、G-5 分離自產品水。
營養瓊脂、假單胞菌瓊脂基礎培養基 /CN 瓊脂、平板計數培養基 /PCA 瓊脂、乙酰胺培養基、乙酰胺肉湯(廣東環凱微生物科技有限公司);RAPID’P.aeruginosa Agar(BIO-RAD)。
VITEK 2 Compact 30 全自動細菌鑒定及藥敏分析係統(梅裏埃);基質輔助激光電離解析飛行時間質普(MALDI-TOF MS Biotyper System)(布魯克);1 ~ 1000 μL 移液器(Eppendorf);LDZX-50KBS 型立式壓力蒸汽滅菌器(上海申安);VORTEX-6 渦旋振蕩儀(其林貝爾)。
1.2 試驗方法
1.2.1 菌株活化
將-80 ℃保存的5株標準菌株與5株實驗室保存菌株劃線接種於營養瓊脂平板上,於36 ℃培養24 h,連續傳代2次,得到活化菌株[14]。
1.2.2 不同選擇培養基特異性比較
(1)特異性比較。將10株菌株分別劃線接種在營養瓊脂、CN瓊脂、乙酰胺培養基、RAPID’s P.aeruginosa Agar4種培養基上,36 ℃培養24 h,比較4種培養基對試驗菌株的特異性。
(2)適用性比較。將10株菌株製成不同濃度(10-2~10-6 CFU)的菌懸液,按照GB 8538—2016的方法對水樣進行過濾,將濾膜轉至營養瓊脂、CN瓊脂、乙酰胺培養基、RAPID’s P.aeruginosa Agar4種培養基上,36 ℃培養24 h,觀察比較對試驗菌株在4種培養基上的生長狀況及顯色反應。
1.2.3 人工模擬汙染試驗
如表1所示,將2~4種菌混合,製備成10-1 CFU的混合菌懸液,梯度稀釋至10-5 CFU,取0.2 mL菌液加入250 mL模擬水樣中,按照GB 8538—2016的方法對水樣進行過濾,將濾膜轉至乙酰胺培養基及RAPID’s P.aeruginosa Agar,36 ℃培養24 h,觀察、比較兩種培養基的檢驗效果。

1.2.4 VITEK 2 Compact全自動細菌鑒定及藥敏分析係統鑒定方法
將活化後的菌株進行革蘭氏染色,於光學顯微鏡下觀察菌體形態及染色結果,根據染色結果和菌體形態選擇相應的鑒定卡。用一次性接種環挑取待測菌株單菌落至含3 mL 0.45% NaCl溶液的一次性懸浮試管中,調節麥氏濃度至0.5~0.6左右,填充對應鑒定卡,采用VITEK 2 Compact全自動細菌鑒定及藥敏分析係統進行係統鑒定。
1.2.5 基質輔助激光電離解析飛行時間質譜(MALDI-TOF MS Biotyper System)鑒定方法根據MALDI-TOF MS Biotyper System操作規程,用一次性接種環挑取新鮮待測菌株單菌落塗布於MALDI靶板,滴加1 μL濃度為70%的甲酸溶液,室溫下晾幹,覆蓋1 μL基質液,室溫下自然晾幹後上機測定。
1.3 數據處理
MALDI-TOF鑒定結果用Biotyper 3.1 database分析;其餘結果采用Excel 2007進行數據統計和分析。
2 結果與分析
2.1 不同選擇培養基特異性比較
2.1.1 特異性比較
10株菌株在4種培養基上培養24 h後的生長狀況如表2所示。由表2可知,在營養瓊脂、CN瓊脂及乙酰胺瓊脂培養基上,銅綠假單胞菌菌落無法與其他的假單胞菌和大腸菌群區分開來;在RAPID’s P.aeruginosa Agar上,銅綠假單胞菌呈現藍綠色,其他菌種在該培養基上不生長或菌落顏色呈白色或淡黃色,可有效、快速的區分銅綠假單胞菌與其他菌群。
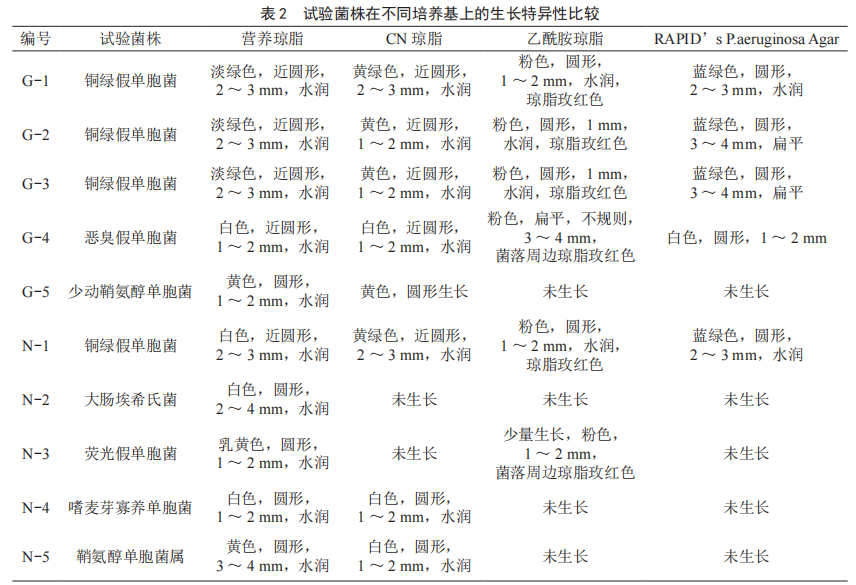
2.1.2 適用性比較
由表3可知,通過不同菌濃度的試驗可知,膜片上高濃度銅綠假單胞菌可能會使乙酰胺培養基呈玫紅色,低濃度銅綠假單胞菌不一定會使培養基呈玫紅色;標準菌株顯色效果要優於從水源水中檢出銅綠假單胞菌;此外,惡臭假單胞菌可使乙酰胺培養基變色呈玫紅色。因此,實際操作中在乙酰胺培養基上無法直接有效區分銅綠假單胞菌與其他的菌落。不同菌濃度樣品的濾膜在RAPID’s P.aeruginosa Agar上表現一致,銅綠假單胞菌呈藍綠色,其他菌種在該培養基上不生長或菌落顏色呈白色或淡黃色。因此,如使用濾膜法進行銅綠假單胞菌的檢測,若使用乙酰胺培養基進行篩選,有可能會造成結果假陰性或假陽性的出現。而在RAPID’s P.aeruginosa Agar上的試驗,濾膜法與直接劃線法結果一致。

2.2 人工模擬汙染試驗分析
RAPID’s P.aeruginosa Agar上,銅綠假單胞菌呈藍綠色,幹擾菌不生長或呈白色,其他菌不會幹擾其在膜片上的生長;而乙酰胺培養基上不能分辨出銅綠假單胞菌與其他菌落。
2.3 VITEK 2 Compact全自動細菌鑒定係統鑒定結果
所有菌株均為革蘭氏陰性菌株,VITEK 2 Compact全自動細菌鑒定係統鑒定結果見表4。VITEK 2 Compact全自動細菌鑒定係統對5株標準菌株的鑒定結果符合率為100%,其餘5株保存菌株中G-1(99%)、G-2(98%)、G-3(99%)鑒定為銅綠假單胞菌。10株菌株中陽性菌株為4株,陰性菌株為6株,4株銅綠假單胞菌全部被檢出。

2.4 基質輔助激光電離解析飛行時間質普(MALDI-TOF MS)鑒定結果
10株菌經MALDI-TOF MS鑒定得到的結果與VITEK 2 Compact全自動細菌鑒定所得鑒定結果一致,如表4所示。
2.5 銅綠假單胞菌檢驗方法的優化及驗證
結合人工模擬汙染試驗與兩種不同鑒定係統的檢驗結果,對銅綠假單胞菌檢驗方法進行適當優化,如圖1所示。優化後的檢驗程序主要分為兩部分:①參考GB 8538—2016的方法對水樣進行過濾,將濾膜轉至RAPID’s P.aeruginosa Agar培養基上,36 ℃培養22~30 h;②利用VITEK 2 Compact全自動細菌鑒定係統對RAPID’s P.aeruginosa Agar平板上典型藍綠色菌落進行鑒定。以檢驗程序兩部分的結果均為陽性時,判定為銅綠假單胞菌,其餘結果為陰性。

采用優化後的方法對1.2.3中的人工模擬汙染試驗水樣進行驗證試驗,結果如圖2所示。優化後的方法在快速識別銅綠假單胞菌與其他幹擾菌(呈白色)的同時,實現了疑似菌落的快速鑒定。所得鑒定結果與傳統鑒定方法一致。

3 結論與討論
銅綠假單胞菌作為一類致病性較低但耐藥性強的細菌,可以長期在水環境中生存,是水質監測的重要指標之一。隨著銅綠假單胞菌汙染飲用水及耐藥性等問題的逐漸突出,選擇適合生產企業的簡便、準確、高效的快速檢測方法,已成為當前產業界和保障人們世界杯賽程預測的迫切需求。現有國標中使用的傳統方法涉及濾膜過濾、微生物培養觀察鑒別及驗證、氧化酶試驗、產氨試驗等,由於試驗過程操作煩瑣、工作量大、成本高且耗時長,已難以滿足當前世界杯賽程預測生產的需求。而針對假單胞菌的選擇性的開發是一個長期的挑戰。此外,不同檢測技術(或方法)的有效性、適用性及相互之間的融合性也成為了提升檢測效率和質量的關鍵。隨著微生物快速檢測技術的不斷進步,VITEK 2 Compact全自動細菌鑒定係統和基質輔助激光解析電離飛行時間質譜技術(MALDI-TOF-MS)已被廣泛用於常規試驗微生物,特別是銅綠假單胞菌的檢測與鑒定[15-17]。
為快速、有效地區分銅綠假單胞菌與其他幹擾菌,本研究通過對不同選擇性培養基檢測效果進行比較發現,乙酰胺瓊脂上銅綠假單胞菌的特異性較差,會出現假陽性或假陰性結果,而銅綠假單胞菌顯色培養基(RAPID’s P.aeruginosa Agar)憑借其典型的菌落特征以及較短的增菌時間,適合對大批量樣品進行快速判定。VITEK 2 Compact全自動細菌鑒定係統及其所攜帶的分析係統可在快速完成菌種鑒定的同時對獲得數據結果進行分析,操作過程安全、快速、準確、重複性好[18-19]。目前,該係統已被應用於中華人民共和國國家標準中關於沙門氏菌、單增李斯特氏菌和副溶血性弧菌的檢驗過程中[20-22]。但是,在日常檢驗工作中按照GB 8538—2016方法和GB 7918.4—1987方法檢測得到的部分陽性菌株在采用VITEK 2 Compact係統進行鑒定時會有一定概率呈現假陽性或假陰性結果,從而會對實際生產中的水質鑒定結論產生誤導。推測其原因在於部分樣品中的陽性菌株在培養過程中因其細胞代謝產物理化性質的差異導致了VITEK 2 Compact係統中個別生化顯色反應的變化從而導致係統的誤判。因此,在采用VITEK 2 Compact係統進行鑒定時,使用快速有效的特異性顯色培養基培養作為對照以減少假陽性或假陰性誤差是十分必要的。
此外,基質輔助激光電離解析飛行時間質普(MALDI-TOF MS)因其對致病菌識別速度快等優勢也在微生物檢測領域得到了推廣應用。崔學文等[23]應用MALDI TOF MS對不同來源的15株銅綠假單胞菌及8株幹擾菌進行鑒定,所得鑒定結果於VITEK完全一致。李進等[24]利用MALDI TOF MS對VIM型和SPM型金屬酶銅綠假單胞菌進行檢測分析,MALDI-TOF MS對25株VIM型菌株靈敏度為92.0%,對於20株SPM型菌株靈敏度為80.0%,所得結果比常規PCR技術更有優勢。但是,由於MALDI-TOF MS具有極高的靈敏度,為避免試驗誤差影響,對於試驗所用的耗材、標準溶劑以及試驗器具的質量要求較高。同時,由於該檢測需要涉及使用專業計算機軟件對所得質量圖譜與標準菌株圖譜庫進行比對鑒定和各種數據的聚類分析,因此對於檢測人員的技術和業務素養要求也較高。再加之整套係統的設備成本,使得該方法目前還難以在廣大的中小企業中得以普及應用。
因此,銅綠假單胞菌顯色培養基(RAPID’s P.aeruginosa Agar)憑借其典型的菌落特征以及較短的增菌時間,將該培養基與VITEK 2 Compact係統結合使用可有效提高檢測效率、準確率、特異性及時效性,適用於對大批量樣品進行快速判定。但考慮到本研究所采用的試驗檢測樣本來源和數量的局限性,這一方法還需通過後續對大量實際樣本的檢測應用來積累數據,以期為我國的飲用水安全保障事業提供技術支持。
參考文獻
[1]Morrison A J,Wenzel R P.Epidemiology of infections due to Pseudomonas aeruginosa[J].Clin Infect Dis,1984,6:S627-S642.
[2]Stover C K,Pham X Q,Erwin A L,et al.Complete genome sequence of Pseudomonas aeruginosa PAO1, an opportunistic pathogen[J].Nature,2000,406:959-964.
[3]Hesse C,Schulz F,Bull C T,et al.Genome-based evolutionary history of Pseudomonas spp[J].Environ Microbiol,2018,20(6):2142-2159.
[4]Kerr K G,Snelling A M.Pseudomonas aeruginosa:a formidable and ever-present adversary[J].J Hosp Infect,2009,73(4):338-344.
[5]Gomez M,Prince A.Opportunistic infections in lung disease: Pseudomonas infection in cystic fibrosis[J].Current Opinion in Pharmacology,2007,7(3):244-251.
[6]Jimenez S.A review of reported recalls involving microbiological control 2004-2011 with emphasis on FDA considerations of ‘objectionable organisms’[J].American pharmaceutical review,2012,15:42-57.
[7]美國食品與藥品管理局.細菌學分析手冊[M].北京:中國輕工業出版社,1986.
[8]Smith R F,Dayton S L.Use of acetamide broth in the isolation of Pseudomonas aeruginosa from rectal swabs[J].Applied Microbiology,1972,24(1):143-145.
[9]Szita G,Gyenes M,Soós L,et al.Detection of Pseudomonas aeruginosa in water samples using a novel synthetic medium and impedimetric technology[J].Letters Applied Microbiology,2007,45:42-46.
[10]衛生部.化妝品微生物標準檢驗方法 綠膿杆菌:GB 7818.4—1987[S].北京:中國標準出版社,1987.
[11]國家衛生和計劃生育委員會,國家食品藥品監督管理總局.世界杯賽程預測 國家標準 飲用天然礦泉水檢驗方法:GB 8538—2016[S].北京:中國標準出版社,2016.
[12]中華人民共和國國家衛生和計劃生育委員會.世界杯賽程預測 國家標準 包裝飲用水:GB 19298—2014[S].北京:中國標準出版社,2014.
[13]黃茜,劉豔,尹佳,等.包裝飲用水中銅綠假單胞菌汙染狀況調查研究[J].中國衛生檢驗雜誌,2019,29(15):1890-1892.
[14]東秀珠,蔡妙英.常見細菌係統鑒定手冊[M].北京:科學出版社,2001.
[15]楊晶,王偉歡.VITEK 2 Compact係統的應用及鑒定結果分析[J].中國衛生檢驗雜誌,2016,26(18):2643-2645.
[16]Pereira F D,Bonatto C C,Lopes C A,et al.Use of MALDI-TOF mass spectrometry to analyze the molecular profile of Pseudomonas aeruginosa biofilms grown on glass and plastic surfaces[J].Microbial Pathogenesis,2015,86:32-37.
[17]楊明,塗鳳琴,胡筱靜,等.銅綠假單胞菌檢測方法研究進展[J].食品工業科技,2019,40(19):345-352.
[18]張帆,李樹垚,張子豪,等.銅綠假單胞菌檢測方法的比較與優化[J].生物技術通報,2018,34(3):67-74.
[19]郭瑞軍.VITEK 2 Compact及其在食品微生物檢測中的應用研究[J].現代食品,2020,12(65):192-201.
[20]國家衛生和計劃生育委員會,國家食品藥品監督管理總局.世界杯賽程預測 國家標準 食品微生物學檢驗 沙門氏菌檢驗:GB 4789.4—2016[S].北京:中國標準出版社,2016.
[21]國家衛生和計劃生育委員會,國家食品藥品監督管理總局.世界杯賽程預測 國家標準 食品微生物學檢驗 單核細胞增生李斯特氏菌檢驗:GB 4789.30—2016[S].北京:中國標準出版社,2016.
[22]國家衛生和計劃生育委員會.世界杯賽程預測 國家標準 食品微生物學檢驗 副溶血性弧菌檢驗:GB 4789.7—2013[S].北京:中國標準出版社,2013.
[23]崔學文,羅慧萍,李增婷,等.基質輔助激光解吸附電離飛行時間質譜在銅綠假單胞菌鑒定中的應用[J].現代預防醫學,2016,43(10):1862-1867.
[24]李進,黎敏,魯衛平.MALDI-TOF MS技術對VIM型和SPM型金屬酶銅綠假單胞菌的檢測分析[J].第三軍醫大學學報,2020,42(16):1663-1669.
基金項目:陝西省科學院科技計劃項目(2018nk-03);西安市科技計劃項目(2020KJRC148)。
作者簡介:單萌(1985—),女,遼寧沈陽人,本科,中級工程師。研究方向:食品微生物風險評估。
通信作者:馬瑜(1982—),女,陝西西安人,博士,副研究員。研究方向:應用生物技術。
熱點推薦
- 2022世界杯32强赛程表时间
- 2022世界杯预选赛
-

全球食品創新平台第五期已啟動,攜手共創安全、健康、綠色的未來
-
特醫食品不是藥,卻是臨床治療的關鍵支撐
- 世界杯2022赛程时间表最新
-

銅綠假單胞菌快速檢測方法的優化研究
-

黴菌酵母快速檢測測試片的優化
-

食品檢測實驗室的內部質量控製方式分析
-
食品中黃曲黴毒素B1檢測方法研究
-

多重PCR法檢測5種動物源性成分的適用性驗證
-
還原劑濃度對氫化物原子熒光法測量飲用水中鉛的影響
-
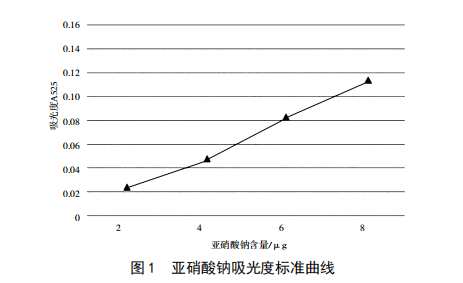
醬菜醃漬類食品亞硝酸鹽含量的檢測
-
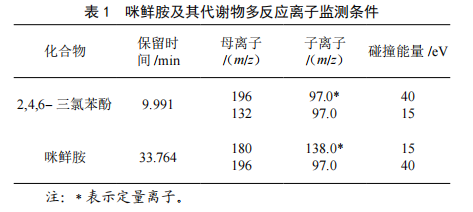
氣相色譜-三重四極杆質譜法測定辣椒中咪鮮胺及其代謝物殘留量
-
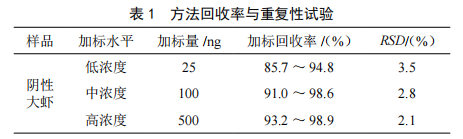
液相色譜-原子熒光法測定水產食品中的甲基汞
-

利用HPLC內標法測定益生菌類保健食品中低聚木糖的含量
-
ATP生物熒光增幅法在食品微生物汙染檢測中的應用
-

高效液相色譜儀、酶標儀和快檢儀檢測小麥中嘔吐毒素的對比分析
-
高效液相色譜法測定烤魚中的苯並[α]芘
-
食品中黴菌檢測方法的改進研究
-
超高效液相色譜法測定不同香型白酒中乳酸和乙酸的含量
-
不同前處理方法對蔬菜、水果農藥殘留GC-MS/MS檢測結果的影響分析
-
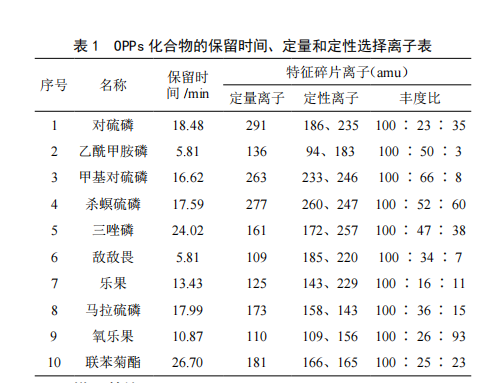
氣相色譜-質譜聯用法測定白花蛇舌草中10種有機磷農藥殘留量
-
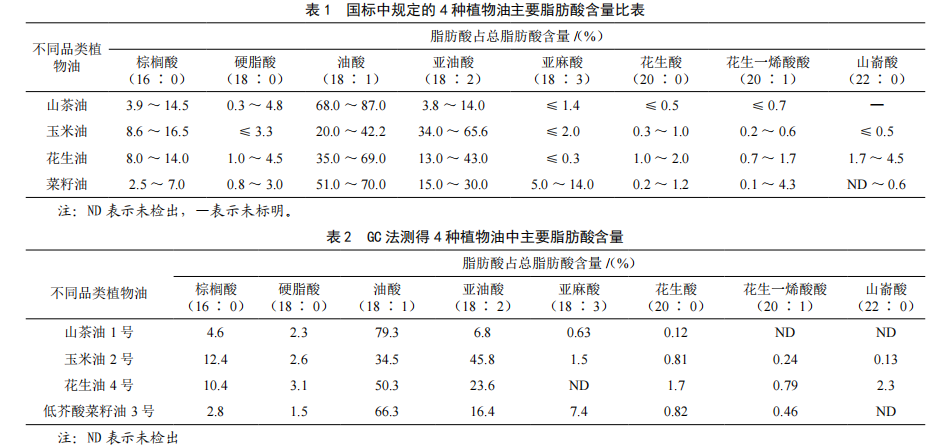
基於GC和GC-MS技術檢測山茶油摻偽
-
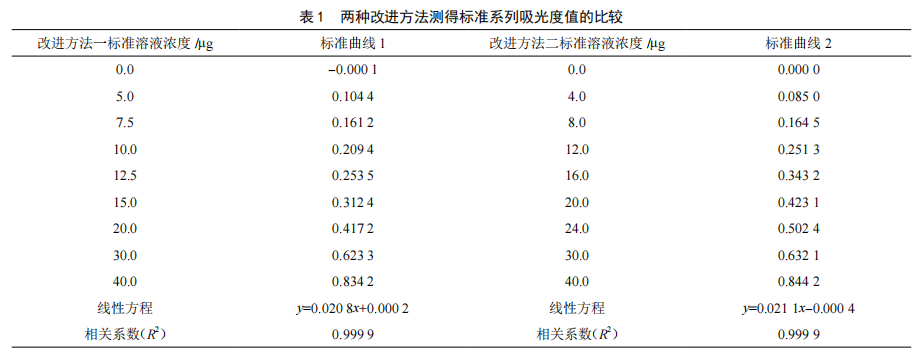
分光光度法測定食品中亞硝酸鹽含量標準曲線線性範圍的研究
-
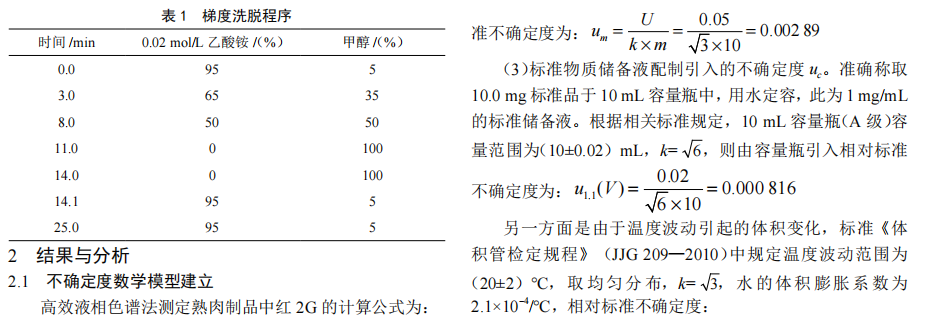
高效液相色譜法測定熟肉製品中非法添加物紅2G的不確定度評定
-

離子色譜法測定天然礦泉水中溴酸鹽的不確定度評定
-
基於多光譜圖像技術的食品質量檢測方法
-
應用拉曼光譜技術開展乳製品安全快檢的探討
-

運用質控數據評定農產品檢測中的測量不確定度
-
2,6-二氯酚靛酚滴定法與碘量法測定蔬菜水果中維生素C




