肉豬體內組織和體液中多西環素含量的相關性研究
2021-10-14 11:26:12 來源: 世界杯賽程預測 導刊
肉豬體內組織和體液中多西環素含量的相關性研究
餘軍軍1,2,藍棋浩1,2,寧 軍1,2,韋 田1,2,梁立傑3,孫 堅3
(1.溫氏食品集團股份有限公司,廣東新興 527400;2.廣東省畜禽健康養殖與環境控製企業重點實驗室,
廣東新興 527400;3.華南農業大學獸醫學院,廣東廣州 510642)
基金項目:2019年廣東省鄉村振興戰略專項資金項目(2019B020401)。
作者簡介:餘軍軍(1986—),男,河南信陽人,碩士,獸醫師。研究方向:獸用藥物代謝動力學與殘留檢測技術。
摘 要:采用液相色譜串聯質譜分析法,對肉豬體內組織(肌肉、肝髒、腎髒、肺髒)和體液(尿液、血液)中多西環素含量進行檢測,分析多西環素在豬體內組織和體液中的殘留消除情況,探討多西環素在體液與各組織殘留量的相關性,並預測達到休藥期時體液中多西環素的含量範圍。結果表明,豬混飲多西環素後各組織中藥物代謝快,體液中藥物濃度低,休藥期為11 d,體液與各組織間藥物殘留量呈較高相關性。當尿液多西環素含量低於57.07 μg/L、血液低於2.76 μg/L時,預測99%動物體內組織中多西環素殘留量低於最大殘留限量,為肉豬宰前監測體內多西環素殘留提供了一種簡單經濟的方法。
關鍵詞:多西環素;豬;殘留消除;休藥期;宰前監測
多西環素(Doxycycline,DOX)是由土黴素在6-位脫氧而製成的第二代半四環素衍生物,又名強力黴素或脫氧土黴素,由美國輝瑞製藥廠在上世紀60年代發明[1]。多西環素是廣譜抗生素,對腸球菌、肺炎球菌、沙門氏菌、大腸杆菌、金黃色葡萄球菌、衣原體、支原體和立克次氏體等具有良好的抗菌效果[2]。因其在體內具有分布廣、長效、高生物利用度和無明顯腎毒性等特點,臨床上廣泛應用於豬、牛、雞和羊的養殖,以治療呼吸道、消化道和泌尿道的細菌性疾病。隨著多西環素在獸醫臨床上的使用,其殘留問題也越來越被重視。目前,國內外對多西環素在動物體內的殘留消除的研究已有很多,但對多西環素在體內的殘留監控主要用動物的可食用組織,尿液和血液中多西環素殘留的消除及殘留監控較少[3-4]。本文通過計算多西環素在豬體內的休藥期,並預測休藥期豬尿液和血液中藥物殘留量範圍,以探索尿液或血液樣品用於多西環素殘留監控的可操作性。
1 材料與方法
1.1 材料
1.1.1 儀器設備
液質聯用儀(QTRAP 5500,美國AB SCIEX公司);組織勻漿機(HM6300,北京Lab Precition公司);氮吹儀(MV5,北京萊伯泰科公司);電子分析天平(BT125D,德國Sartorius公司);冷凍高速離心機(5804R,德國Eppendorf公司);C18固相吸附劑(月旭科技公司);6cc/200 mg的固相萃取小柱(Oasis HLB,美國Waters公司)。
1.1.2 試劑
多西環素對照品,純度97.2%,批號1-F-4F4-1,美國CATO公司;多西環素-D3對照品,純度97%,批號T291402,加拿大TRC公司;甲醇、乙腈和甲酸均為色譜純,購於德國默克公司;正己烷、三氯乙酸為分析純,購於廣州化學試劑廠;鹽酸多西環素可溶性粉,獸藥字190172193,含量10%,批號20191004,購於河北遠征禾木藥業有限公司。
1.1.3 試驗動物的飼養與管理
選擇健康、體重相近的三元雜商品豬41頭(40.5±3.8) kg,隨機分成2組,分別為對照組1頭,試驗組40頭。試驗組在基礎飲水中添加鹽酸多西環素可溶性粉,製成多西環素濃度為50 mg/L的藥液,連續混飲給藥5 d。於停藥後第1 d、2 d、3 d、5 d、8 d、12 d、15 d和18 d隨機選擇5頭豬隻,采集組織(肌肉、肝髒、腎髒、肺髒)和體液(尿液、血液)作為檢測
樣品。
1.2 試驗方法
1.2.1 溶液配製
(1)多西環素儲備液(1 000 μg/mL).準確稱取50.0 mg多西環素對照品,置於50 mL容量瓶中,用甲醇溶解並定容至刻度,搖勻密封,置-20 ℃冰箱中保存。
(2)多西環素-D3儲備液(100 μg/mL)。準確稱取1.0 mg多西環素-D3對照品,置於10 mL容量瓶中,用甲醇溶解並定容至刻度,搖勻密封,置-20 ℃冰箱中保存。
(3)三氯乙酸(1 mol/L)。準確稱取16.3 g三氯乙酸置於100 mL容量瓶中,加入超純水溶解並定容至刻度,搖勻。
1.2.2 樣品處理
(1)組織。稱取2.0 g勻漿後的組織樣品置於50 mL離心管中,加入50 μL內標溶液(濃度5 μg/mL),靜置
5 min。然後加入2 mL水、8 mL乙腈。渦旋混勻後,超聲提取10 min。然後室溫條件下4 000 r/min離心5 min,上清液倒入50 mL離心管中,加入500 mg C18吸附劑,渦旋30 s
淨化。再重複離心1次,移取5 mL上清液在50 ℃水浴中氮氣吹幹。殘渣中加入1 mL甲醇水(10︰90)、2 mL正己烷,渦旋30 s。室溫條件4 000 r/min下離心10 min,吸取下層過0.22 μm濾膜,待測。
(2)尿液:取5 mL尿液樣品於15 mL離心管中,並加入20 μL內標溶液(濃度5 μg/mL),靜置10 min。將HLB萃取小柱固定在固相萃取裝置上,依次用5 mL甲醇、5 mL超純水活化後,倒入尿液樣品,用5 mL水、5 mL甲醇水(20︰80)淋洗,抽幹,5 mL甲醇洗脫,收集洗脫液。洗脫液在在50 ℃水浴中氮氣吹幹,殘渣用1 mL甲醇水(10︰90)溶解,渦旋30 s。樣品過0.22 μm濾膜,待測。
(3)血液。準確吸取500 μL血漿,依次加入20 μL內標(5 μg/mL)、500 μL三氯乙酸溶液,渦旋混勻,10 000 r/min室溫條件下離心10 min,上清液過0.22 μm針頭濾膜,待
上機。
1.2.3 儀器條件
(1)色譜條件:Waters Acquity UPLC BEH C18色譜柱
(2.1 mm ×50 mm,1.7 μm);流速:0.25 mL/min;流動相:A為0.1%甲酸溶液,B為甲醇;梯度洗脫條件:0~2 min,
5%~15% B;2~5 min,15%~40% B;5~7 min,40%~95% B;7~7.1 min,95%~5% B;7.1~12 min,5%。柱溫為35 ℃。進樣體積為10 μL。
(2)質譜條件:電噴霧離子源(ESI);多反應監測(MRM)正離子模式;離子源溫度550 ℃;電噴霧電壓(IS)5.5 kV;氣簾氣壓力(CUR)、霧化氣壓力(GS1)及輔助氣壓力(GS2)分別為35 kPa、55 kPa和60 kPa。藥物優化的去簇電壓和碰撞能量等質譜參數見表1。
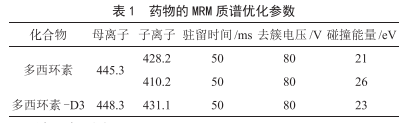
2 結果與分析
2.1 組織中多西環素殘留消除規律
不同時間點各組織中多西環素殘留量見表2。結果顯示,10%多西環素可溶性粉按推薦劑量連續用藥5 d後,多西環素在肝髒和腎髒中的殘留含量最高,在肌肉、肺髒中的含量較低,停藥2 d後,多西環素在肌肉和肝髒的殘留量分別為(99.30±33.84)μg/kg和(104.51±29.20)μg/kg,均低於最高殘留量MRL[5](肝髒300 μg/kg,肌肉100 μg/kg),停藥3 d後,腎髒中的多西環素殘留量為(350.28±136.12)μg/kg,低於了最高殘留量MRL(腎髒600 μg/kg)。多西環素主要殘留部位在腎髒,各組織中殘留消除的速度較快,在停藥後5 d,組織中均檢測不出多西環素。在停藥8 d采集的5頭豬血液中,隻有1份樣品檢出多西環素。
2.2 休藥期計算
按照農業部對多西環素最大殘留限量[5]和歐盟對休藥期計算方法,利用WT1.4軟件按雙單側99%置信區間計算多西環素在豬組織中休藥期[6]。由圖1可知,多西環素在肌肉中的休藥期為10.58 d、肝髒為10.80 d、腎髒為8.13d、肺髒為10.51 d,考慮到給藥方式等因素的影響,建議休藥期為11 d。
2.3 體液中多西環素殘留量相關性研究
通過統計學軟件SPSS,采用統計學軟件SPSS,對雙變量“停藥後體液中多西環素含量”“各組織中多西環素含量”進行相關性分析。由表3可知,停藥後體液中多西環素殘留量與各組織中多西環素殘留量之間的相關係數大於0.85,相關係數的顯著性水平為0.01,體液與各組織中多西環素殘留量之間是高度相關的。



2.4 組織中藥物殘留量低於MRL時體液中殘留量區間預測
使用SPSS軟件對時間-體液中藥物濃度進行線性分析,並根據建立的模型預測停藥為10.80 d時的體液中藥物濃度區間範圍。結果顯示,當時間為10.80 d時,即肉豬體內組織中多西環素殘留量低於最大殘留限量時,尿液中藥物濃度區間範圍為57.07~252.12 μg/L;血液中藥物濃度區間範圍為2.76~28.68 μg/L。


3 結論與討
目前,常用的動物體內藥物殘留檢測方法包括微生物法、毛細管電泳法、酶聯免疫法、液相色譜法和液相色譜串聯質譜法等,其中液相色譜串聯質譜法作為唯一確證方法應用最多。龐國芳等[7]采用液相色譜串聯質譜法檢測了體內各組織和體液中多西環素的殘留量,製定了該產品的休藥期為11 d,為藥物的臨床使用提供了數據支持。
劉欣[3]按體重10 mg/kg的劑量給予鹽酸多西環素顆粒,每天1次,連續5 d,研究多西環素在動物體內的消除規律,結果顯示,停藥後第3天,除1頭豬肝髒組織中的殘留量高於MRL外,其他各組織中藥物的殘留量均低於MRL,同時計算休藥期為12 d[8-9]。而本試驗結果中,停藥後第3天,豬各組織中藥物殘留量均低於MRL,計算休藥期為11 d,翟克影[4]也做了相關研究,除了劑型和給藥方式不同,鹽酸多西環素在豬體殘留分布與消除結果基本相似。
在實際生產中,通過對豬活體尿液樣品的檢測,建立的回歸方程,可以間接判斷豬體內多西環素殘留量是否低於最大殘留限量。20世紀末開始已有不少學者采用這種經典回歸法來預測組織中藥物的殘留濃度,但在研究時均沒有考慮個體間差異,試驗的重複性較差[10]。本文根據停藥後尿液、血液中藥物消除情況,引入置信區間預測,考慮了個體間差異,通過計算發現當動物停藥時間到達休藥期時,尿液中多西環素殘留量區間下限為57.07 μg/L、血液為2.76 μg/L,表明可通過監測體液中多西環素濃度判斷動物體內組織中藥物殘留量是否安全。考慮到尿液樣品獲取更便捷,采取時動物應激更小,動物屠宰前可檢測尿液判斷動物是否符合屠宰要求,判定限為57 μg/L。
參考文獻
[1]趙嬋娟.多西環素研究進展[J].湖北畜牧獸醫,2012(12):
10-14.
[2]操繼躍.豬呼吸係統感染性疾病藥物治療[J].養殖與飼料,2005(4):39-43.
[3]劉欣,魏麗娟,瞿紅穎,等.鹽酸多西環素顆粒在豬體內殘留消除的研究[J].黑龍江畜牧獸醫,2017,539(23):201-203.
[4]翟克影.鹽酸多西環素可溶性粉在豬體內藥物動力學及殘留研究[D].武漢:華中農業大學,2008.
[5]中華人民共和國農業農村部,國家衛生健康委員會,國家市場監督管理總局.
世界杯賽程預測國家標準 食品中獸藥最大殘留限量:GB 31650—2019[S].北京:中國標準出版社,2019.
[6]Nahler M.Committee for veterinary medicinal products (CVMP)[J].Springer Vienna,2009,296:9-10.
[7]龐國芳.獸藥多組分殘留分析技術[M].北京:科學出版社,2016.
[8]Chiesa L,Nobile M,Arioli F,et al.Determination of veterinary antibiotics in bovine urine by liquid chromatography-tandem mass spectrometry[J]. Food Chemistry,2015,185(15):7-15.
[9]Junior L B,Leal M G,Uchoa F,et al.Determination of quinine and doxycycline in rat plasma by LC–MS–MS:Application to a pharmacokinetic study[J].Chromatographia,2011,73(11):1081-1088.
[10]黃顯會,蔡勤仁,劉戎,等.克倫特羅在豬組織和尿液中殘留消除規律研究[J].動物毒物學,2003,18(1):32-37.
熱點推薦
- 2022世界杯预选赛
-

全球食品創新平台第五期已啟動,攜手共創安全、健康、綠色的未來
-
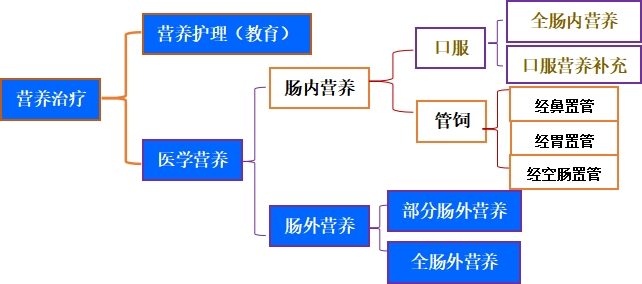
特醫食品不是藥,卻是臨床治療的關鍵支撐
- 世界杯2022赛程时间表最新
-

全十紅紅稗餅幹|中秋團圓,回家必備
-

肉豬體內組織和體液中多西環素含量的相關性研究
-
一起因食用韭菜餅引起亞硝酸鹽食物中毒原因的實驗室分析
-
茯磚茶中特征揮發成分分析
-

GC-MS/MS法測定芹菜中毒死蜱殘留量 不確定度評定
-
免疫親和柱-高效液相色譜法測定餅幹中赭曲黴毒素A的含量
-

國際FAPAS乳粉中金黃色葡萄球菌定量檢測能力驗證結果與分析
-

液相色譜-串聯質譜法測定芝麻油中乙基麥芽酚
-
微波消解-ICP-MS和高壓封閉消解-ICP-MS測定農產品中16種元素的方法研
-

高效液相色譜法測定飲料中的阿力甜含量
-

雙歧杆菌在嬰兒配方奶粉中的穩定性研究
-

石墨爐自動標準加入法與標準曲線法測定牛肉醬中的鉛比較
-
基於熒光PCR檢驗方法對食品中沙門氏菌檢驗的分析研究
-
和田地區蔬菜中農藥殘留汙染情況調查與分析
-

大型農產品集中交易市場快檢準確性調查分析
-
高效液相色譜法快速測定腐乳中誘惑紅的方法研究
-
超高效液相色譜-串聯質譜法同時測定小麥中4種真菌毒素
-

關於微生物法測定米粉中維生素B6含量不確定度評估
-

加強食品質量監督檢驗數據真實性和有效性的路徑
-

食品微生物檢測方法及質量控製對策探究
-
大學生世界杯賽程預測 關注度及相關知識認知調查
-

食品檢驗在保障世界杯賽程預測 中的重要性探究
-
大型超市食品零售的經營模式與質量管理研究
-

生物傳感快速檢測技術的探討
-

淺談我國餐飲產業鏈中央廚房中預製菜
-
淄博市2015—2019年食源性疾病暴發事件流行病學特征分析





