濕式大腸菌群快檢紙片性能驗證的方法探索
2021-08-30 14:51:57 來源: 世界杯賽程預測 導刊
濕式大腸菌群快檢紙片性能驗證的方法探索
劉 哲,李丹妮,王 宇,王 濤,王 萌,馮 淑
(延安市食品質量安全檢驗檢測中心,陝西延安 716000)
作者簡介:劉哲(1989—),男,漢族,陝西延安人,本科,助理工程師。研究方向:食品檢驗。
摘 要:目的:探索對市售濕式大腸菌群快檢紙片性能進行分析、驗證的一般流程,為檢測、監測機構、企業和個人選用、驗收該類快檢產品提供參考。方法:從紙片的汙染指標、特異性指標、檢出水平(LODX)、檢測結果有效性和產品質量穩定性等方麵進行試驗研究,對紙片的性能進行綜合分析和驗證。結果:紙片的各項試驗結果基本符合預期和產品自身的質量要求。結論:本文所探索的對濕式大腸菌群快檢紙片性能進行分析驗證的一般流程可有效對該類紙片產品進行較為全麵的性能驗證,在使用該類快檢產品時可作為產品選用和驗收、驗證的參考。
關鍵詞:大腸菌群;快檢紙片;性能驗證
大腸菌群是指一類在一定培養條件下能夠發酵乳糖、產酸產氣的需氧或兼性厭氧革蘭氏陰性無芽孢杆菌[1]。濕式大腸菌群快檢紙片是近年來新出現的可用於餐(飲)具或公共場所用品用具大腸菌群檢測的快檢產品,該類產品具有攜帶方便、操作簡單等特點,且相較於幹式快檢紙片省去了使用無菌生理鹽水潤濕紙片的環節,從而降低了檢測操作和環境汙染的風險[2]。
近年來,隨著各類快檢產品出現的越來越多,各產品的質量也參差不齊[3-4],產品使用單位或個人對所購買產品的性能缺乏有效了解。本文將著重探索對濕式大腸菌群快檢紙片的性能進行分析、驗證的一般流程,為產品使用單位或個人選用和驗收、驗證該類大腸菌群快檢產品提供參考。
1 材料和方法
1.1 材料與試劑
環境樣本(自然環境、居住、辦公環境等)、人工汙染樣本。濕式大腸菌群快檢紙片、月桂基硫酸鹽胰蛋白腖肉湯(LST)、煌綠乳糖膽鹽肉湯(BGLB)、營養肉湯(NB)、營養瓊脂(NA)、無菌接種環、無菌移液管、無菌平皿等。
標準菌株:大腸埃希氏菌(ATCC 25922)、弗氏檸檬酸杆菌(ATCC 43864)、產氣腸杆菌(ATCC 13048)、福氏誌賀氏菌(CICC 21534)、鼠傷寒沙門氏菌(ATCC 14028)、糞腸球菌(ATCC 29212)和金黃色葡萄球菌(ATCC 6538)。
1.2 儀器與設備
生物安全櫃、冰箱(2~8 ℃)、培養箱(36±1)℃、渦旋振蕩器、移液槍等。
1.3 方法
本文將著重對紙片的汙染指標、特異性指標、檢出水平(LODX)、檢測結果有效性和產品質量穩定性驗證等方麵進行試驗分析。
1.3.1 汙染指標
選取2~4個不同批號(本次試驗為4個批號:200605、200903、210505和210506)的濕式大腸菌群快檢紙片產品,無菌操作,每個批號分別取5張快檢紙片,裝入紙片配套的無菌小袋中,置(36±1)℃培養箱中培養18 h,觀察結果。
1.3.2 特異性指標
本文綜合濕式大腸菌群快檢紙片自身的產品質量要求和《
世界杯賽程預測國家標準 食品微生物學檢驗 培養基和試劑的質量要求》(GB 4789.28—2013)中對大腸菌群相關培養基、試劑的質量要求,確定使用大腸埃希氏菌、弗氏檸檬酸杆菌、產氣腸杆菌、福氏誌賀氏菌、鼠傷寒沙門氏菌、糞腸球菌和金黃色葡萄球菌等7種菌對紙片進行大腸菌群的特異性驗證。
驗證時,用無菌接種環從上述7種菌的新鮮營養瓊脂斜麵上沾取一環菌,直接於紙片表麵劃線,然後置於(36±1)℃培養箱中培養18 h,觀察各菌在紙片上的特異形態。本文試驗中選取了4個不同批號(同1.3.1)的紙片進行特異性驗證。
1.3.3 檢出水平(LODX)
本文通過紙片對高、中、低3個接種水平和空白的樣本勻液的測試結果來獲得該紙片法的檢出水平(由於測試的樣品數量較少,本文中使用“估計LOD50”[5]),高、中、低3個接種水平和空白分別做2個測試,共獲得8個結果。記錄每個接種水平獲得的陽性結果(檢出)數量,使用《微生物檢測方法確認與驗證指南》(RB/T 033—2020)附錄B中的表B.1確定估計LOD50。
高水平接種量為不超過預期LOD50(預期的LOD50設定為:≤3 CFU/測試單元[5])的10倍,中水平接種量可由高水平接種物稀釋2倍獲得,低水平接種量可由高水平接種物稀釋10倍獲得。
用大腸埃希氏菌(ATCC 25922)製備濃度(單位:CFU/mL)分別為高、中、低接種水平10倍的接種物勻液。測試時,無菌操作,先取適量濕式大腸菌群快檢紙片置於配套的無菌袋中,然後分別吸取0.1 mL(測試單元)各接種水平的接種物勻液和空白液,均勻滴加(接種)於紙片表麵,每個接種水平和空白分別測試2張紙片,滴加(接種)完成後,將紙片置於(36±1)℃培養箱中培養18 h,觀察結果。同時,分別吸取0.1 mL各水平接種物勻液和空白液加入2個無菌平皿,立即倒入15~20 mL冷卻至46 ℃的營養瓊脂,搖勻,(36±1)℃培養24 h,計數,對各接種水平的接種物勻液濃度和空白對照進行同步確認。觀察並記錄測試結果。
1.3.4 檢測結果有效性
本文試驗中,為覆蓋更廣泛的微生物種類,用濕式大腸菌群快檢紙片對采集的21個自然環境(土壤、河流、小溪等)樣本、30個居住環境(廚房、餐廳、衛生間和臥室等)樣本和20個辦公環境(辦公室、走廊、電梯間、公共衛生間等)樣本,共計71個環境微生物樣本進行檢測,然後將所有的檢測結果用《
世界杯賽程預測國家標準 消毒餐(飲)具》(GB 14934—2016)中的附錄B B.1發酵法進行確認,從而對紙片的檢測結果有效性進行驗證。
操作時,環境表麵的微生物樣本直接用紙片進行采集,土壤、河流等不適合直接采集微生物的樣本,加無菌生理鹽水振蕩提取其中的微生物後,取適量提取液置營養肉湯(NB)中培養過夜,再取樣本培養液劃線接種於紙片,(36±1)℃培養18 h,記錄檢測結果。液體樣本直接取適量樣本勻液經肉湯增菌後,取增菌液劃線接種於紙片。
無菌操作,將培養後的紙片全部分別轉移至LST肉湯管,置培養箱中(36±1)℃培養24~48 h,進行發酵試驗。後續複發酵試驗和結果判定按GB 14934—2016附錄B B.1發酵法中的要求進行。觀察並記錄測試結果。
1.3.5 產品質量穩定性
同一生產批號的紙片可通過在常規條件下保存3~6個月以上後再次進行汙染指標和特異性指標的驗證來分析該紙片在產品有效期內的質量穩定性,本次試驗選取已於常規保存條件下保存11個月的濕式大腸菌群快檢紙片(生產批號:200605)進行驗證。不同生產批號紙片質量的持續穩定性由1.3.1~1.3.3的試驗中,同時或先後選取2~4個不同批號的紙片進行驗證。
2 結果與分析
2.1 汙染指標
試驗中4個不同批號的紙片經(36±1)℃培養18 h後,均無變化,保持初始的狀態和顏色(濕潤、平整,紫色)。表明在無菌操作及規定的培養條件下,紙片和配套的無菌塑料小袋自身不會出現汙染而幹擾大腸菌群檢測。
2.2 特異性指標
試驗結果顯示,3種大腸菌群(大腸埃希氏菌、弗氏檸檬酸杆菌和產氣腸杆菌)在紙片上生長旺盛,且呈現典型的陽性反應,即紙片上可見點、線狀紅色斑點或片狀紅暈,斑點周圍變黃或明顯變黃。其他4種菌中,鼠傷寒沙門氏菌和福氏誌賀氏菌呈陰性反應,即紙片上可見點、線狀紅色斑點或片狀紅暈,但斑點或紅暈周圍顏色不變。另外2種革蘭氏陽性菌處於被抑製狀態,隻可見少量紅色斑點或紅暈且斑點或紅暈周圍不變色,呈陰性反應,且各菌在不同批號紙片上的特異形態無明顯區別。說明本次試驗中該紙片對大腸菌群和非大腸菌群細菌可呈現明顯的特異性反應,且對革蘭氏陽性菌有一定抑製作用。
2.3 檢出水平(LODX)
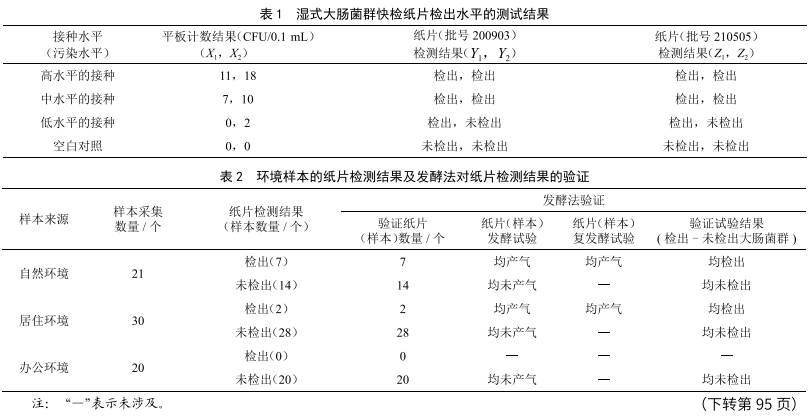
檢出水平的測試結果見表1。結果表明,紙片在樣品(接種物勻液)處於低汙染水平時,即測試單元(0.1 mL樣液)中的目標微生物數為1CFU((0+2)/2=1)時,即有50%的概率檢出該菌(2張測試紙片中有1張檢出(陽性))。在高汙染水平和中汙染水平時2張紙片均檢出。且2個批號的紙片測試結果一致。查RB/T 033—2020附錄B 表B.1,得估計LOD50(CFU/測試單元)=1 CFU/測試單元。測試結果間接表明該紙片的性能符合預期。
2.4 檢測結果有效性
樣本的紙片檢測結果及發酵法對紙片檢測結果的驗證見表2。結果表明,在本次試驗中,該紙片的檢測結果與發酵法的驗證結果一致,說明對采集到的同一樣本,其與發酵法的檢測結果一致,表明該紙片顯示的檢測結果與發酵法結果同等可靠有效。

2.5 產品質量穩定性
同一批號(200605)的紙片在常規條件下保存11個月之後,其汙染指標和特異性指標試驗結果未發生變化。不同批號的紙片,其汙染指標、特異性指標和檢出水平的測試結果一致(參見2.1~2.3)。
結果表明該紙片不論是同一批號產品在有效期內的質量穩定性,還是不同批號產品質量的持續穩定性均符合預期。
3 結論
本文對選取或設定的濕式大腸菌群快檢紙片的汙染指標、特異性指標、檢出水平(LODX)、檢測結果有效性和產品質量穩定性等5項性能指標進行了較為詳細的試驗分析,證明該紙片性能穩定可靠,符合要求和預期的同時,也表明本文所探索的對濕式大腸菌群快檢紙片性能進行分析驗證的一般流程可有效的對該類紙片產品進行較為全麵的性能驗證,在使用該類快檢產品時可作為產品選用和驗收、驗證的參考。
參考文獻
[1]何國慶,賈英民,丁立孝.食品微生物學[M].北京:中國農業大學出版社,2016.
[2]劉德鵬,郝英敏,薑玉芳.濕式與幹式大腸菌群快檢紙片的應用比較研究[J].醫藥前沿,2015(28):172-174.
[3]王珍,陸雯,吳嶽琴,等.四種大腸菌群快速檢測紙片質量考察[J].現代食品,2019,12(23):138-142.
[4]王讚信.大腸菌群快檢紙片的質量檢測分析[J].預防醫學,2005,17(5):81-82.
[5]國家認證認可監督管理委員會.微生物檢測方法確認與驗證指南:RB/T 033—2020[S].北京:中國標準出版社,2016.
熱點推薦
-
特醫食品不是藥,卻是臨床治療的關鍵支撐
- 世界杯2022赛程时间表最新
-

全十紅紅稗餅幹|中秋團圓,回家必備
-

和汪氏蜂蜜共同來普及蜂蜜結晶現象
-

拿坡海開啟西餐加盟新潮流, 大眾化家庭小西餐成未來新趨勢
-

濕式大腸菌群快檢紙片性能驗證的方法探索
-
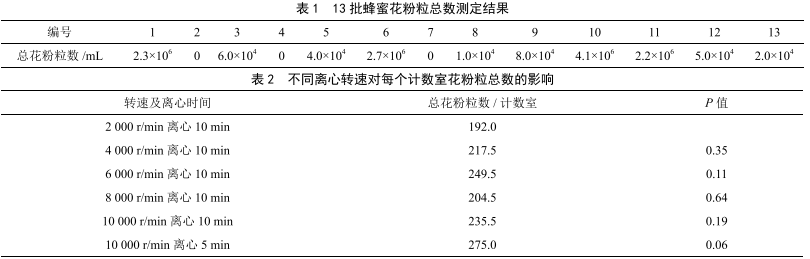
市售蜂蜜中花粉粒總數測定
-

2020年陽江市江城區生活飲用水溶解性總固體和總硬度指標分析
-
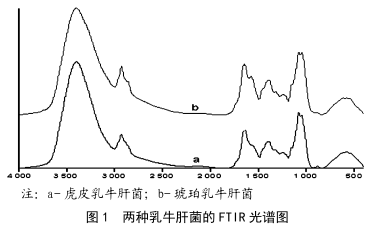
牛肝菌的紅外光譜分析
-

基於高效液相色譜法蔬果中滅多威及異丙威的
-
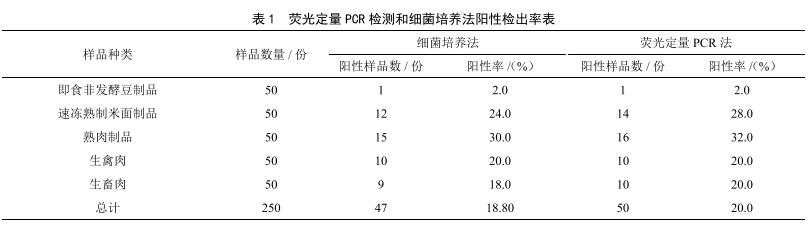
不同方法檢測食源性致病菌的對比研究
-
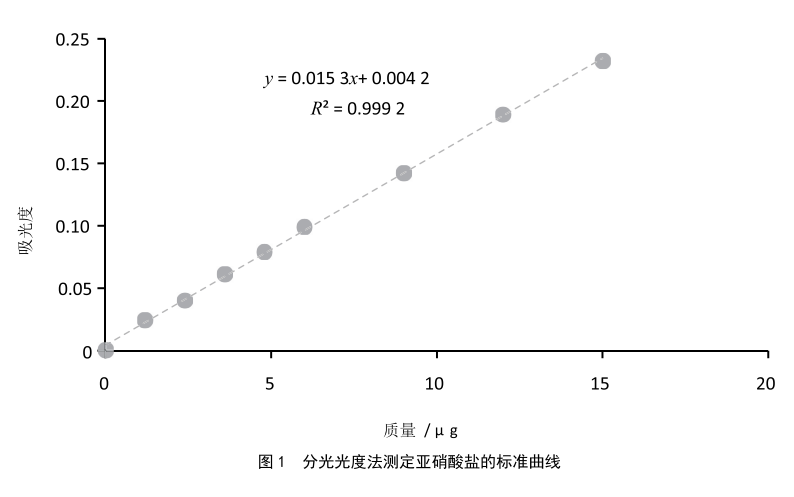
醬醃菜中亞硝酸鹽含量的測定
-
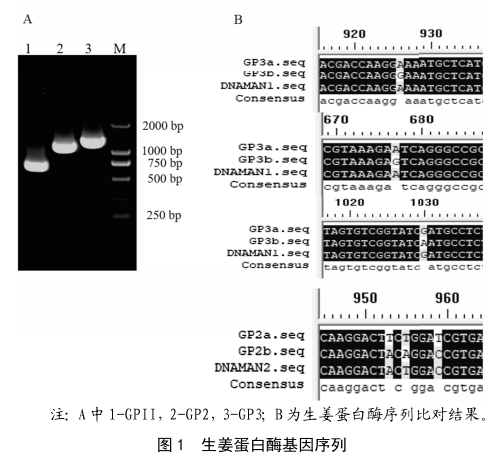
生薑蛋白酶基因的克隆及在原核細胞中的表達
-
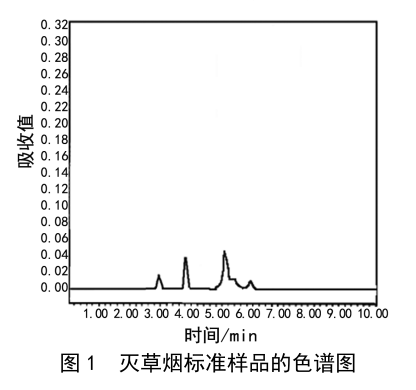
高效液相色譜法測定牛奶中咪唑啉酮類除草劑——滅草煙的含量
-
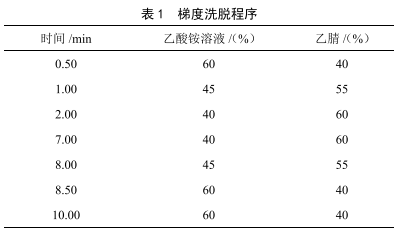
高效液相色譜-串聯質譜法測定蓮菜中
-

2020年慶陽市餐飲服務單位消毒餐飲具大腸菌群分析報告
-

UPLC-MS/MS法測定畜肉中萊克多巴胺
-

2017—2019年煙台經濟技術開發區中小學及托幼機構飲用水調查分析
-

食品鏈中五氯酚酸鈉風險梳理及對策
-

啤酒非生物穩定性及控製簡述
-
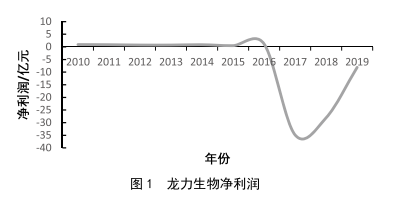
食品企業內部控製風險分析及對策研究 ——以龍力生物為例
-
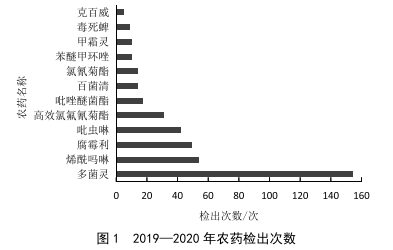
平涼市農產品質量安全現狀及建議
-

珠三角地區肉製品中亞硝酸鹽含量調查分析
-
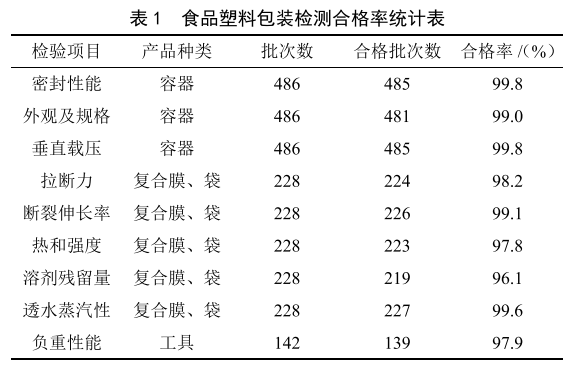
食品用塑料包裝產品質量與世界杯賽程預測
-

冷凍飲品中增稠劑使用情況調查
-
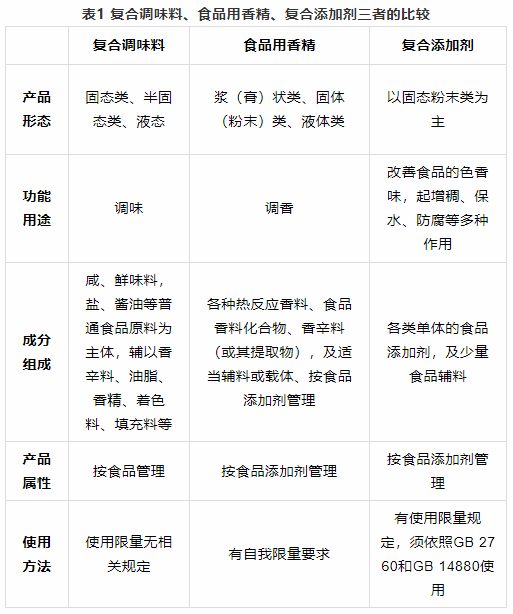
你知道複合調味料、食品用香精與複合食品添加劑的區別嗎?
-
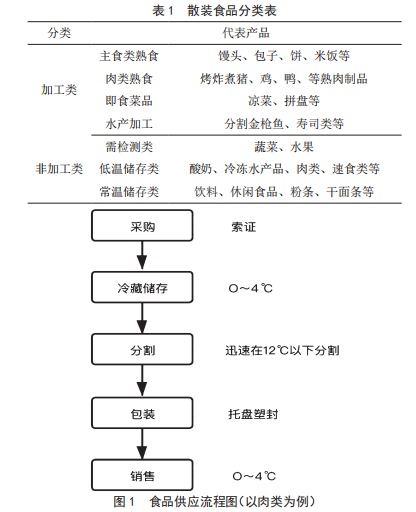
大型超市散裝食品質量管理體係的建立與實踐研究
-
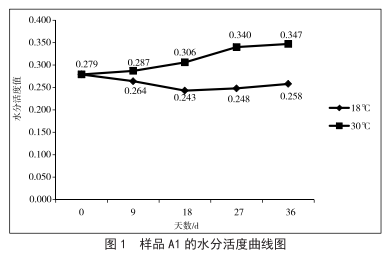
嬰幼兒穀類輔助食品開封後水分活度的變化及安全性評價
-
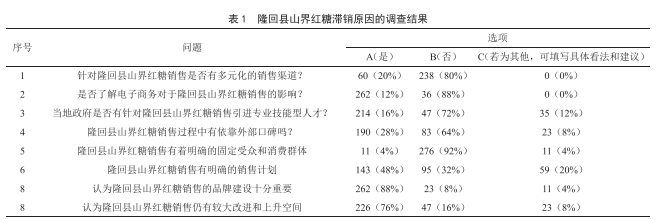
隆回縣山界紅糖滯銷的調查分析與應對建議
-
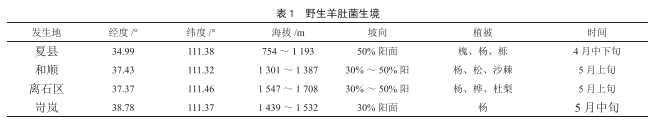
山西部分地區野生羊股菌資源調査





