豬肉中氯丙嗪殘留UPLC-MS/MS檢測法的優化研究
2020-06-11 17:01:26 來源: 世界杯賽程預測 導刊
□ 王婷 錫林郭勒盟食品藥品檢驗檢測中心
摘 要:本文在《豬腎和肌肉組織中氯丙嗪殘留量的測定》(GB/T 20763-2006)的基礎上優化了樣品的提取淨化方式,增加了定性離子,建立了操作便捷、準確度高、重現性好的豬肉中氯丙嗪殘留量液質檢測的新方法。具體操作為,樣品在堿性條件下經特丁基甲醚提取,冷凍離心除脂後取上清液,經液相色譜質譜聯用儀分析檢測。結果表明,優化後的方法在0.5~20ng/mL範圍內線性關係良好,相關係數r=0.9997;在0.5~5μg/kg範圍內,3個濃度的加標回收率均在75%~95%之間,測定結果均滿足國標方法中的重複性要求(含量範圍:0.750~4.800μg/kg、r=0.4736m-0.1775)。
關鍵詞:氯丙嗪 液相色譜-質譜聯用法 殘留量 豬肉
氯丙嗪屬於吩噻嗪類藥物,可作用於中樞神經係統,故被作為中樞多巴胺受體的阻斷劑,具有鎮靜、催眠、鎮吐、抗暈眩等功效[1-3]。當前,氯丙嗪常被一些養殖戶違規添加至家畜飼料中,目的是通過抑製家畜運動來達到“短期育肥”的效果,或在家畜長途運輸過程中減少其應激反應,進而降低死亡率[4-5]。氯丙嗪的藥物濫用造成其在動物體內大量殘留,並通過食物鏈進入人體,長期蓄積會引發人體食物中毒、肝髒和腎髒病變等,直接危害人體健康[6-7]。目前,歐盟及我國相關部門均明令規定“不得在動物源性食品中檢出氯丙嗪”[8-9]。當前,我國對氯丙嗪藥物在食品中的殘留檢測方法主要采用《豬腎和肌肉組織中氯丙嗪殘留量的測定》(GB/T 20763-2006)。經過實驗發現,該檢測方法前處理過程中的提取和淨化操作是通過調節pH值控製目標物在有機相和水相兩相間重複萃取,處理過程繁瑣,特丁基甲醚用量大、次數多,且目標物隨特丁基甲醚使用量的增加而不斷損失,導致回收率偏低。因此,本文對該方法的前處理方法進行改進,優化步驟,建立了操作便捷、準確度高、重現性好的前處理方法,希望為提高氯丙嗪的日常檢驗效率和標準更新提供參考依據。
1 材料與方法
1.1 主要儀器及試劑
1.1.1 主要儀器及設備
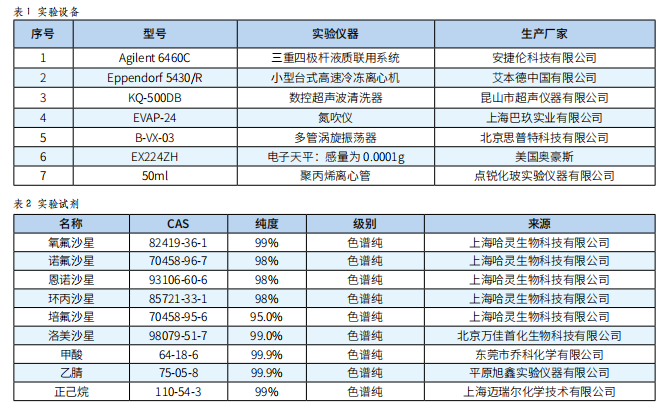
Thermo TSQ QUANTUM ULTRA超高效液相色譜-質譜聯用儀,美國Thermo Fisher科技公司;台式冷凍離心機,鹽城市安信實驗設備有限公司。
1.1.2 試劑及樣品
1.1.2.1 試劑
鹽酸氯丙嗪標準品,購自北京北方偉業計量技術研究院;供試試劑試藥:乙腈、甲酸均為色譜級,氫氧化鈉、特丁基甲醚為優級純,實驗用水為屈臣氏蒸餾水;氫氧化鈉溶液:5mol/L;甲酸水溶液:0.2%(體積分數);鹽酸氯丙嗪標準溶液:100μg/mL。
1.1.2.2 樣品
將市售豬肉攪碎拌勻,密封,待用。
1.2 試驗方法
1.2.1 樣品處理
稱取2.00g(精確到0.01g)均質試樣於50mL離心管中,加入0.2mL乙腈混勻,然後加入5mol/L氫氧化鈉溶液400μL,渦流混合30s。置於80±5℃恒溫水浴中1h,期間進行兩次渦流混合。1h後取出,冷卻至室溫。精密量取1mL特丁基甲醚加入離心管,高速振蕩15min後置於冷凍離心機中離心10min(溫度2℃、轉速10000r/min),取上清液過0.2μm濾膜上機。
1.3 儀器分析方法
1.3.1 色譜條件
色譜柱:Thermo Fisher Hypersil Gold C18(內徑100×2.1mm,粒徑1.7um);柱溫:40℃;進樣體積:5μL;流速:0.2mL/min;流動相A:0.2%甲酸水溶液,流動相B:乙腈。
洗脫程序:0min,B相:5%;0.5min,B相:5%;4min,B相:95%;6min,B相:95%;6.1min,B相:5%;10min,B相:5%。
1.3.2 質譜條件
ESI正離子模式,噴霧電壓3.5kV,蒸發溫度320℃,離子傳輸管溫度300℃,鞘氣(N2)流量35arb,輔助氣(N2)10arb。
氯丙嗪母離子:319.063amu,子離子:58.585amu、86.434amu、214.124amu、246.156amu,86.434amu為定量離子。
2 結果與分析
2.1 樣品前處理優化
按照GB/T 20763-2006中的前處理方法進行提取、淨化,發現氯丙嗪回收率極低。參照標準溯源分析發現,氯丙嗪易溶於特丁基甲醚,故淨化除酯操作過程中,目標物易隨特丁基甲醚流失,從而導致回收率低,故針對上述問題做出如下調整。
①將標準中“加入12mL特丁基甲醚,……,待淨化”改為“精密量取1mL特丁基甲醚加入離心管”,在保證充分萃取的前提下,減少醚類有毒試劑的使用量。
②將原標準淨化步驟:“在上述15mL離心管中加入1mol/L磷酸二氫鉀溶液(pH值=3)3mL,……,超聲處理10min”改為“提取後置於冷凍離心機離心10min(溫度為2℃,轉速為10000r/min)”。經過離心,離心管內液體分為3層——下層為水層、中間層為結塊的油脂、上層為特丁基甲醚,吸取醚層,過0.2μm有機濾膜直接上機測定。
采用優化後的步驟進行前處理,有效避免了原標準提取和淨化操作步驟中目標物在有機相和水相兩相間反複萃取造成的損失,且特丁基甲醚用量大幅降低,優化後的回收率提高至75%~95%,穩定性好,檢測結果的準確性高。
2.2 質譜條件優化
原標準中氯丙嗪的定性子離子為:58.2amu和86.2amu。由於子離子碎片較小,相對豐度差異較大,因此容易出現共流出幹擾。此外,如果出現陽性臨界值樣品,則難以快速準確定性。通過儀器優化,選取58.585amu、86.434amu、214.124amu和246.156amu為定性子離子,多選出來的兩個子離子可用於輔助定性。
2.3 檢測結果分析
2.3.1 線性實驗
精密量取氯丙嗪標準溶液,加入特丁基甲醚製成濃度為0.5、1、2、5、10、20ng/mL的標準點,采用“1.3”中色譜質譜條件進行檢測,測得氯丙嗪線性方程:Y=21341.9+190076X,相關係數R2=0.9997。
2.3.2 方法的靈敏度和穩定性
原標準方法中的氯丙嗪檢出限為0.5μg/kg,本研究采用豬肉空白基質分別按0.5、1、5μg/kg這3個水平進行添加回收實驗,依據上述方法進行測定,測定結果均滿足國標方法中的重複性要求(含量範圍:0.750~4.800μg/kg、r=0.4736m-0.1775),3個水平的陽性添加回收率均在75%~95%之間,回收率穩定。結果顯示,優化後的方法在原標準檢出限0.5μg/kg處可以準確定量。
2.3.3 樣品檢測結果
20批次樣品中均未檢出氯丙嗪殘留。
3 結論
通過對前處理過程中的淨化步驟進行改進,采用冷凍離心除脂代替了調節樣品pH值重複萃取操作,不僅使有毒試劑的使用量減少,而且大幅縮減了操作時間,有效減少目標物的損失。該前處理方法操作簡單,安全性高,結果準確度高、重現性好,靈敏度高於現行標準,故適用於大批量豬肉中氯丙嗪殘留量的檢測。
參考文獻:
[1] 楊曉雲,王立世,莫金垣,等.毛細管電泳安培法同時檢測異丙嗪和氯丙嗪[J].分析化學,1999,27(8):991.
[2] 李向麗,張娜,王文林.食品中安定和氯丙嗪殘留檢測研究進展[J].安徽農業科學,2014,42(2):565-567,580.
[3] 劉建靜,楊曙明.氯丙嗪殘留檢測技術研究進展[J].中國畜牧獸醫,2008,35(10):141-144.
[4] Amaral L,Viveiros M,Molnar J.Antimicrobial activity of Phenothiazines [J].In Vivo,2004,18(6):725-731.
[5] 李樂華,趙靖平,房茂勝,等.齊拉西酮與氟呱啶醇治療精神分裂症隨機雙盲雙模擬多中心對照研究[J].中國新藥與臨床雜誌,2006,26(5):335-338.
[6] 孔紅英.吩噻嗪類抗精神藥物對神經係統的副作用分析及處理[J].中國中醫資訊,2011,3(10):230-230.
[7] 魯桂芳,滕青賢.氯丙嗪不良反應回顧[J].中國醫院用藥評價與分析,2007,7(5):388-390.
[8]李波平,花錦,李涵,等.UPLC-MS/MS法測定3種獸藥製劑中違禁藥物氯丙嗪[J].中國獸藥雜誌,2015,49(5):32-36.
[9] 《世界杯賽程預測國家標準 食品中獸藥最大殘留限量》(GB31650-2019)農業農村部、國家衛生健康委員會和國家市場監督管理總局公告2019年第114號.2019-09-06.
熱點推薦
-

全十紅紅稗餅幹|中秋團圓,回家必備
-

和汪氏蜂蜜共同來普及蜂蜜結晶現象
-

拿坡海開啟西餐加盟新潮流, 大眾化家庭小西餐成未來新趨勢
-

摩購空間“霸王餐”來襲 打破傳統營銷套路帶動商家業績翻倍
-

開學季食安隱患猛增 禧雲食安開展公益行動助力意識提升
-
肉製品中喹諾酮殘留檢測
-

庫爾班大叔一夜之間變“網紅” 一米長的烤串供不應求
-

吃雞已經OUT,現在最流行看球吃鴨!
-

低於成本叫賣的牛肉幹 當心是走私肉
-

東方紫:戈壁灘披荊斬棘 讓天山“無抗”雪雞飛入尋常百家
-

舟曲從嶺藏雞: 來自海拔3800米,北緯34度無可替代的稀世珍品
-

從源頭保證肉製品的安全
-

攜手推動世界杯賽程預測 倡議,規範禽肉食品質量安全管理
-

肉製品安全與質量檢測,任重而道遠
-

庖丁解“肉”:“紅”與“白”的困惑
-

普通豬價上漲 高檔“土肉”爭打折市場
-
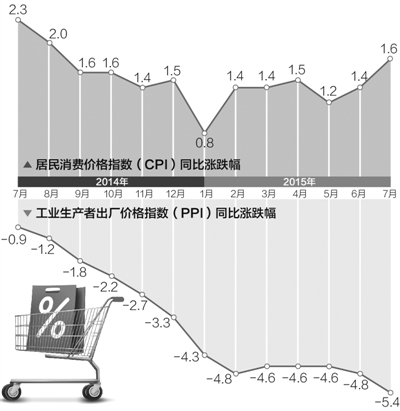
豬肉和旅遊價格上漲是CPI環比上漲主因
-
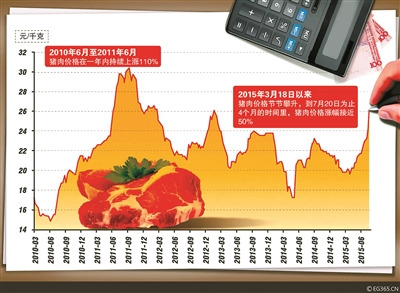
豬肉價格創下三年內新高 最近數月漲幅已超30%
-

記者調查凍肉銷售鏈條 商家:換個包裝就可以賣
-

怕吃“僵屍肉” 越南人棄食凍雞爪
-
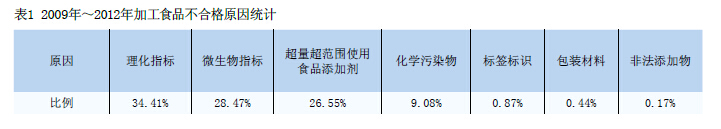
中國肉類食品質量安全控製問題淺談
-
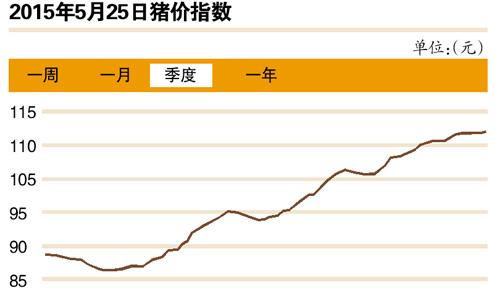
5月豬股伴豬價齊“飛” 可能助推CPI上漲
-

今年清明乳豬價格下降 團購價是市價一半是否有貓膩
-

活雞“遭休” 凍雞“受寵”
-

低溫肉製品在市場脫穎而出 雙彙和雨潤誰是老大
-

不同部位的牛肉怎樣搭配葡萄酒?
-

選對雞肉、注意衛生,預防沙門氏菌食物中毒
-

標準化助推肉類食品行業發展
-

肉製品加工廠產品出廠前編寫檢驗報告
-

筋道肉丸多加肉彈素 這樣的肉丸能吃嗎?





