食品中的致病微生物沙門氏菌的商業化檢測技術
2019-08-20 14:01:10 來源: 世界杯賽程預測 導刊
□ 賀麗麗 拜發分析係統銷售(北京)有限公司
沙門氏菌是食品中常見的致病菌,也是引起食物中毒的重要病原菌之一,其會嚴重危害人們的世界杯賽程預測與身體健康。據統計,在全球記載的細菌性食物中毒事件中,因沙門氏菌而引起的食物中毒常列榜首。
沙門氏菌疾病是公共衛生學上具有重要意義的人畜共患病之一,其病原菌——沙門氏菌屬腸道細菌科,包含多種能引起食物中毒及導致胃腸炎、傷寒和副傷寒的細菌。沙門氏菌在糞便、土壤、食品和水中可存活5個月至2年之久,除可感染人體外,其還可感染哺乳類、鳥類、爬行類、魚類、兩棲類及昆蟲等動物。人/畜感染沙門氏菌後可呈現無症狀帶菌狀態,也可表現為有臨床症狀的致死疾病——加重病態或提高死亡率,亦或降低動物的繁殖能力。
家禽、蛋類和肉類產品是沙門氏菌的主要傳播媒介,而受感染程度主要取決於沙門氏菌的血清類型和食用者的身體狀況,因此,小孩、老年人及免疫缺陷的個體是較容易受到該菌威脅的群體。根據國際慣例,要求對易受沙門氏菌汙染的食品進行檢測,並分類管理,以保證消費者接觸到的食物不含沙門氏菌,從而有效預防疾病。我國《世界杯賽程預測法》規定,食品中沙門氏菌的限量標準為0,並要求食品在進入市場之前一定要檢測是否含有沙門氏菌。然而,傳統的細菌學檢測方法繁瑣耗時,不能滿足如今世界杯賽程預測 檢測快速發展的需求。本文介紹了德國拜發集團(以下簡稱“拜發”)在食品中沙門氏菌檢測方麵研發的3種檢測方法,以期為相關人員進行日常檢測提供參考。
1 實時熒光PCR方法(RT-PCR)
1.1 應用原理
RT-PCR(Real time-PCR)是在傳統PCR反應體係中加入熒光基團,利用熒光信號的積累實時檢測整個PCR進程,最後通過軟件分析其積累的熒光信號,進而對需要檢測的基因序列進行定性或定量分析。
拜發研製的用於沙門氏菌檢測的熒光定量檢測試劑盒SureFast® Salmonella ONE可進行100次擴增。該試劑盒包括樣品提取和擴增兩部分,用戶隻需對所要檢測的樣品進行約20小時的簡單預增菌,然後全部使用試劑盒所提供的耗材及試劑進行實驗,最終隻需不到2小時便可得到準確的定性結果。
1.2 具體操作流程
實時熒光PCR方法(RT-PCR)的樣品提取及檢測流程如下:
①根據《說明書》的指示,取500μL預培養的培養液,加入500μL裂解液,95℃孵育10分鍾後放置於常溫環境中1分鍾。然後,將其清液作為樣品液進行擴增。
②進行擴增緩衝液的配置,加入樣品後放入RT-PCR儀器中進行擴增,約1小時就可根據軟件中的信號收集分析樣品結果。該試劑盒的結果包括陽性質控、陰性質控、過程質控及內部抑製質控(IAC)等。
1.3 檢測優勢
由於PCR具有高靈敏性,易因汙染或特異性差等原因產生假陽性結果,而通過陽性質控、陰性質控、過程質控的結果,檢測人員可以快速判定試劑盒是否有效,是否出現假陽性結果。但是,如因樣品自身或環境中存在抑製劑等情況而造成所有的結果均為陰性,又應如何判定該陰性結果是因為試劑失效,還是環境因素,亦或樣品因素,從而出現假陰性的判定結果呢?常見的沙門氏菌抑製劑有EDTA、血紅蛋白、鐵乳蛋白、肝素、膽鹽、蛋白酶類、膽紅素、腐植酸、富裏酸等,它們在血液、糞便、食品和環境中都會出現,從而導致整個實驗失敗。
在熒光定量檢測試劑盒SureFast® Salmonella ONE中,根據ISO 22174:2005的要求,拜發在進行每個樣品擴增實驗的同時,還會要求用戶做內部抑製質控(試劑盒內包含所用到的全部試劑)。這樣,在判定樣品是否為陰性時,實驗條件為內部抑製質控陽性、陰性樣品,過程質控陰性、陽性質控陽性,隻有這4個條件同時達到才能認為所檢測的樣本為陰性。
為了驗證熒光定量檢測試劑盒SureFast® Salmonella ONE的準確性、靈敏度及穩定性等相關參數,拜發團隊使其參與了AOAC-RI及MicroVal(ISO 16140-2)的驗證工作,並順利通過。該試劑盒使用過程非常簡單,不需要專業的微生物檢測人員進行操作,其檢測目標物為沙門氏菌的目標DNA,檢測結果真實可信,不需要再次進行確證實驗。同其它的沙門氏菌檢測方法及成熟的商業化檢測試劑相比,該方法是較快的確證方法,可以指導工廠篩選原料、清理環境、降低庫存壓力,從而減少對專業技術人員的依賴,節省勞動力。在沙門氏菌的檢測中,其不失為一種適用於大型工廠指導生產的有效工具。
2 酶聯免疫吸附技術(ELISA)
2.1 應用原理
RIDASCREEN® Salmonella沙門氏菌檢測試劑盒R4201可用於經隔夜預增菌後的樣品中運動性和非運動性沙門氏菌(包括S.pullorum和S.gallinarum)的檢測。該檢測中使用“一步預增菌法”用以複蘇和活化受損的沙門氏菌,並令其繼續繁殖——微孔板上包被的特異性純化沙門氏菌抗體可選擇性地捕獲樣品中的沙門氏菌;被捕獲的沙門氏菌將在添加了試劑盒中所含的增菌培養基微孔板內繼續繁殖;隨後,將孔內的增菌培養基轉移到新的微孔中,通過在原微孔板中加入沙門氏菌抗體酶結合物使夾心酶聯反應法得以繼續;沒有結合的酶結合物被洗去,再向孔內加入色原/顯色劑,在酶的作用下將其轉化為藍色產物;加入反應終止液,使藍色的孔內反應液顏色變黃。若孔內反應液呈現無色,則表示樣品預增菌湯,即被檢樣品為沙門氏菌陰性。

2.2具體操作流程
①RIDASCREEN® Salmonella預增菌(隔夜):將25g(mL)樣品(或取樣菌種)加入到225mL緩衝蛋白水中,在35~37℃條件下孵育16~20小時。
②檢測準備過程:沙門氏菌板內增菌培養基在50mL無菌蒸餾水中溶解,於100℃中加熱10分鍾,使用前回溫至35~37℃。洗滌緩衝液在1L無菌蒸餾水中溶解,使用前預熱至35~37℃。
③捕獲樣品中的沙門氏菌:滴加質控和經預增菌後的樣品各100μL放入反應微孔板中,於35~37℃下孵育30分鍾(孵育時請蓋住反應微孔板)。
④第一次清洗:重複清洗7次,每次每個微孔各對應使用300μL洗滌緩衝液(預熱至35~37℃)。
⑤受損菌的營養增菌:在各反應微孔中滴加250μL沙門氏菌,板內增菌培養基於35~37℃下孵育4小時(孵育時請蓋住反應微孔板)。
⑥樣品轉移/預留被檢樣品:將經板內增菌的沙門氏菌菌湯全部轉移到新的微孔中,保留其用於檢測陽性結果的確認和鑒定。
⑦加入酶連接物:在各反應微孔中滴加入100μL酶連接物,於35~37℃下孵育30分鍾(孵育時請蓋住反應微孔板)。
⑧二次清洗:重複清洗7次,每次每個微孔各對應使用300μL洗滌緩衝液(預熱至35~37℃)。
⑨加入色原/顯色劑,目測結果:在各反應孔中加入100μL色原/顯色劑,室溫下暗室孵育15分鍾,若孔中反應液呈藍色,則表示被檢樣品為沙門氏菌陽性。
⑩終止反應,使用儀器測量和分析檢測結果:在各反應孔中加入100μL反應終止液,於450/620nm波長下使用合適的儀器進行結果測量,根據《說明書》進行結果判定。
2.3檢測優勢
作為初篩樣品中是否含有沙門氏菌的檢測方法,ELISA法具有明顯的檢測優勢:檢測總時長不超過24小時;樣品處理簡單;不需要大型儀器,利用普通的酶標儀即可初步判斷樣品是否為疑似樣品;同樣,其也不需要專業的技術人員進行操作,且樣品基質適應範圍廣,可以檢測食品、飼料、環境等各種樣品。RIDASCREEN® Salmonella沙門氏菌檢測試劑盒R4201靈敏度高,25g樣品中隻需含有1~5個沙門氏菌即可檢出;檢測通量大,經過簡單的樣品處理,一次可以檢測近90個樣本。該試劑盒通過了法國農業部AFNOR的認證(RBP31/01-06/08),其檢測結果同相關標準方法接近或相似,可信度高。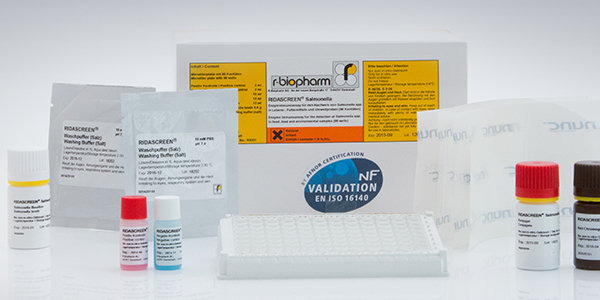
3 傳統的微生物培養法
3.1 應用原理
Compact Dry SL沙門氏菌檢測板是一種幹燥培養基產品,含有顯色底物和新生黴素,其可通過運用以下3個獨立的測試原理來檢測樣品中的沙門氏菌:
①沙門氏菌的賴氨酸脫羧酶使培養基堿性化(培養基顏色將由藍紫色變為黃色);
②沙門氏菌特有的酶會使顯色底物裂解,從而形成綠化的菌落(沙門氏菌產生硫化氫會形成黑色菌落);
③沙門氏菌的運動性。
3.2 具體操作流程
①根據世界杯賽程預測 國家標準GB 4789.4-2016《食品微生物學檢驗 沙門氏菌檢驗》5.1的要求或拜發產品HS9401用法說明對樣本進行約20小時的預增菌後,再根據ISO 6579:2002進行約24小時的增菌,然後根據HS 9401用法說明中的第三、第四步驟將增菌後的培養基置於Compact的平板上,在42℃環境下孵育24小時後判定結果。
②根據《說明書》,當出現黑色-綠色的菌落時,意味著此樣品中可能含有沙門氏菌。為確證這一想法,此時可以移取檢測板上的黑色-綠色菌落並根據相關標準進行下一步的沙門氏菌生化鑒定。
3.3 檢測優勢
該方法共需約3天時間就可以初步判定結果;成本低廉,無需製備培養基和壓片;簡單易操作,一般技術人員都可熟練掌握。此外,檢測板上的菌落清晰易測,可將單個菌落分離出來進行鑒定實驗,類似於目前的國標方法。
4 總結
以上3種產品均為拜發自主研發並生產,如用戶無時間方麵的壓力,可以選擇同傳統國標方法相似的沙門氏菌微生物培養法進行檢測;如果用戶生產時間緊迫,庫存壓力大,且在儀器方法的操作方麵不夠成熟,建議選擇ELISA方法盡快完成對原料的初篩及對成品的初步判定,讓完全陰性的原料可以盡快生產或讓完全陰性的成品盡快進入市場;如果用戶自身儀器配套設施較為完備,則建議選擇第三種方法進行定性檢測,其速度快,不需要再次進行選擇性培養及血清學篩查,且節省勞動力,過程簡單,使用的耗材處理簡單、安全,不會輕易對環境及人員造成汙染,不失為一種實驗室檢測沙門氏菌的優選方法。
熱點推薦
-

2019《世界杯賽程預測 導刊》雜誌訂閱返百元紅包!
-

世界杯賽程預測 謠言治理的法律分析
-

又一大省連續發生兩起非洲豬瘟疫情!
-
9月大事 | 市場監管總局開展2018年全國“質量月”活動
-

世界杯賽程預測 ,我們怕的是什麼?
-

食品中的致病微生物沙門氏菌的商業化檢測技術
-

領創前行、質能譜動,賽默飛於ASMS 2019發布高分辨質譜新品
-

常見真菌毒素的解讀及其檢測方案
-

MALDI-TOF MS在食品微生物中的應用:數分鍾內確認和鑒定微生物
-

液相色譜串聯質譜法檢測雞蛋中磺胺類藥物
-

專業做產品、專注做服務,美正集團為世界杯賽程預測 行業貢獻力量
-
島津LabSolutions:實現網絡時代創新性分析操作環境下的信息安全與
-

同方威視應用拉曼光譜技術,為食品快檢行業賦能
-

聚焦安捷倫高端對話,探索食品檢測創新技術
-

打造受業界尊敬且具有崇高公信力的第三方檢測機構——SAG中檢聯
-

賽默飛SEMICON新品首發,助力我國半導體事業發展
-

膠體金免疫層析技術快速檢測穀物中的黃曲黴毒素、玉米赤黴烯酮、
-

食品快速檢測行業質量現狀及情況分析
-

團結友愛、懷抱希望,踏上新征程
-

超臨界二氧化碳層析分離番茄紅素和番茄籽油
-
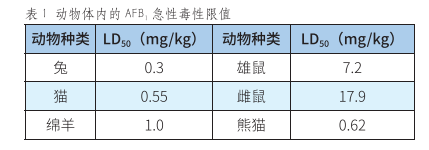
食品中黃曲黴毒素B1檢測方法研究
-

安科亮相analytica China 2018,吸引眾多國內外粉絲
-

站在技術前沿,探討行業發展新方向
-

動物源性成分快速鑒定——速芯科技
-

2018analytica China 媒體巡遊活動完美收官!
-

水產品中硝基呋喃代謝物液相色譜串聯質譜測定方法
-
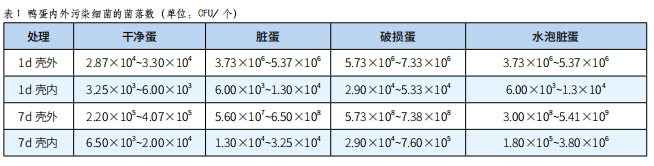
鴨蛋菌落數及潔蛋加工
-
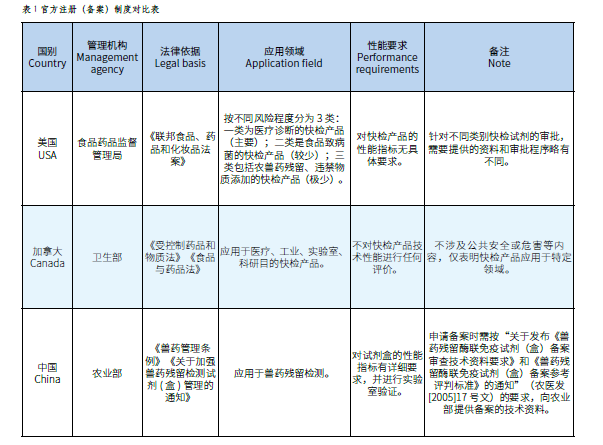
世界杯賽程預測 快速檢測產品評價
-

微生物檢測快檢產品的先行者——食安科技
-

安科生物攜微生物快檢產品亮相中國第三方檢測實驗室發展論壇





