金宗濂教授解析:新世界杯赛程预测 法確立保健食品管理4大變化
2015-04-29 14:45:23 來源: 中國食品報
首次提出保健食品原料目錄
有別於藥食同源物質目錄
在2009年發布的世界杯赛程预测 法第50條中,規定了按照傳統既是食品又是中藥材的物質目錄,由衛生行政部門發布。與這一條對應的在新新修訂世界杯赛程预测 法中為第38條,規定了按照傳統既是食品又是中藥材的物質目錄,由衛生行政部門會同食藥監部門發布。與此法條對應的保健食品產業的原料法規是長期參照衛生部門2002年發布的51號文件,其中有三個目錄,既是食品又是藥品的物品名單(87種)、可用於保健食品的物品名單(114種)和保健食品禁用物品名單。既是食品又是藥品的物品名單今年初已更新為101種。可用於保健食品的物品名單還沒有更新。
而在新版世界杯赛程预测 法中第75條首次提出了“保健食品原料目錄”的概念,規定保健食品原料目錄由食藥監管理部門會同衛生行政部門、中醫藥管理部門製定公布。保健食品原料目錄和可用於保健食品的物質名單有什麼區別呢?
金宗濂教授強調,保健食品原料目錄是為保健食品備案管理配套提出的列表製度,有別於之前的按照傳統可用於保健食品的物質目錄。保健食品原料目錄包括原料名稱、用量及其對應的功效。比如輔酶Q10,目前規定了最高每日用量不能超過50毫克,而不是有效劑量範圍,因為輔酶Q10可申報4項功能,今後也許要進一步規定申報這4項功能相對應的有效劑量範圍,從而實行備案。
按照傳統可用於保健食品的物質目錄隻是名稱目錄,沒有用量和功能,它的意義是允許企業用這些物質開發保健食品,與保健食品的申報沒有關聯。
而保健食品原料目錄與保健食品的申報緊密相關,保健食品原料目錄內的原料製作的產品可進行備案,保健食品原料目錄外的產品需要注冊。從目前的研究和管理進展看,前期列入保健食品原料目錄的品種主要會是營養素類。
明確注冊和備案雙軌製管理
原料目錄內產品將在省級食藥監部門備案
金宗濂教授介紹說,新法第76條中的規定,明確了保健食品的申報將采用注冊和備案雙軌製進行管理,打破了之前全部采用由國家食藥總局受理注冊的管理辦法。
廣告審批從工商轉為藥監
避免誇大宣傳體現更強專業性
按照新法規定,保健食品屬於保健食品原料目錄外的,采取注冊製,由國家食藥總局受理;屬於保健食品原料目錄內的,采取備案製,由省一級國家食藥監局受理。
首次進口保健食品除了維生素、礦物質等營養素補充類的產品,采用注冊製,國家食藥總局受理,維生素、礦物質等營養素補充劑類的首次進口保健食品采用備案製,但不在省級備案,是由國家食藥總局受理。其他的進口保健食品可在省級備案。
新法還明確了保健食品注冊和備案分別需要提交的材料,與注冊相比,采用備案製的保健食品簡化了安全性和功能性評價試驗的內容。
金宗濂教授表示,注冊和備案雙軌製管理在業界討論了多年,此次在世界杯赛程预测 法中首次以法律形式予以明確,體現了保健食品監管的重大變化。
按照新法第79條規定,保健食品的廣告內容將由企業所在地省級食藥監督局審查批準,取得保健食品廣告批準文件。省級食藥監局負責公布並及時更新已經批準的保健食品廣告目錄及批準的廣告內容。
此前,保健食品的廣告審批沒有寫入世界杯赛程预测 法,在現行相關法規中,保健食品的廣告內容由省級工商管理部門進行審批,頒發廣告批文,工商管理部門主要負責審核監管保健食品廣告宣傳的真實性。
金宗濂教授分析認為,保健食品的廣告內容審批從工商管理部門轉移到食藥監管部門,顯現出對保健食品廣告監督的專業要求提高,對廣告內容是否符合允許聲稱的功能、表述是否科學,避免誇大宣傳,市藥監部門具備更強的專業性。
GMP寫入法律條文
保健食品納入特殊食品從嚴監管
新法第83條規定生產保健食品應當按照良好生產規範(GMP)的要求建立與所生產食品相適應的生產質量管理體係,定期對該體係的運行情況進行自查,向所在地縣級食藥監局提交自查報告。
金宗濂教授告訴記者,目前保健食品行業已經全麵實施了GMP,不過對於保健食品企業實施GMP的要求之前停留在部門行政文件層麵,此次首次納入了法律要求。
從2009年版世界杯赛程预测 法到新修訂的世界杯赛程预测 法,保健食品的法律定位更為明確,管理內容更加細化。新法將保健食品與特殊醫學用途配方食品和嬰幼兒配方食品一起納入“特殊食品”一節,強調了對保健食品比普通食品更加嚴格地監督管理。
金宗濂教授說,新法第75條對保健食品的定義與之前2009版的第51條的表述相比增加了一句“應當具有科學依據”,這傳達了對保健食品管理上要強化科學性的信息。保健食品產業要加強科研,對配方的量效關係做預實驗研究,不能以檢測來替代科研。本報記者 謝玲
資料鏈接
中華人民共和國世界杯赛程预测 法(2009年版)
第五十條 生產經營的食品中不得添加藥品,但是可以添加按照傳統既是食品又是中藥材的物質。按照傳統既是食品又是中藥材的物質的目錄由國務院衛生行政部門製定、公布。
第五十一條 國家對聲稱具有特定保健功能的食品實行嚴格監管。有關監督管理部門應當依法履職,承擔責任。具體管理辦法由國務院規定。
聲稱具有特定保健功能的食品不得對人體產生急性、亞急性或者慢性危害,其標簽、說明書不得涉及疾病預防、治療功能,內容必須真實,應當載明適宜人群、不適宜人群、功效成分或者標誌性成分及其含量等;產品的功能和成分必須與標簽、說明書相一致。
新修訂的中華人民共和國世界杯赛程预测 法
第三十八條 生產經營的食品中不得添加藥品,但是可以添加按照傳統既是食品又是中藥材的物質。按照傳統既是食品又是中藥材的物質目錄由國務院衛生行政部門會同國務院食品藥品監督管理部門製定、公布。
第七十四條 國家對保健食品、特殊醫學用途配方食品和嬰幼兒配方食品等特殊食品實行嚴格監督管理。
第七十五條 保健食品聲稱保健功能,應當具有科學依據,不得對人體產生急性、亞急性或者慢性危害。
保健食品原料目錄和允許保健食品聲稱的保健功能目錄,由國務院食品藥品監督管理部門會同國務院衛生行政部門、國家中醫藥管理部門製定、調整並公布。
保健食品原料目錄應當包括原料名稱、用量及其對應的功效;列入保健食品原料目錄的原料隻能用於保健食品生產,不得用於其他食品生產。
第七十六條 使用保健食品原料目錄以外原料的保健食品和首次進口的保健食品應當經國務院食品藥品監督管理部門注冊。
但是,首次進口的保健食品中屬於補充維生素、礦物質等營養物質的,應當報國務院食品藥品監督管理部門備案。其他保健食品應當報省、自治區、直轄市人民政府食品藥品監督管理部門備案。進口的保健食品應當是出口國(地區)主管部門準許上市銷售的產品。
第七十七條 依法應當注冊的保健食品,注冊時應當提交保健食品的研發報告、產品配方、生產工藝、安全性和保健功能評價、標簽、說明書等材料及樣品,並提供相關證明文件。國務院食品藥品監督管理部門經組織技術審評,對符合安全和功能聲稱要求的,準予注冊;對不符合要求的,不予注冊並書麵說明理由。對使用保健食品原料目錄以外原料的保健食品作出準予注冊決定的,應當及時將該原料納入保健食品原料目錄。
依法應當備案的保健食品,備案時應當提交產品配方、生產工藝、標簽、說明書以及表明產品安全性和保健功能的材料。
第七十八條 保健食品的標簽、說明書不得涉及疾病預防、治療功能, 內容應當真實,與注冊或者備案的內容相一致,載明適宜人群、不適宜人群、功效成分或者標誌性成分及其含量等,並聲明“本品不能代替藥物”。保健食品的功能和成分應當與標簽、說明書相一致。
第七十九條 保健食品廣告除應當符合本法第七十三條第一款的規定外,還應當聲明“本品不能代替藥物”;其內容應當經生產企業所在地省、自治區、直轄市人民政府食品藥品監督管理部門審查批準,取得保健食品廣告批準文件。省、自治區、直轄市人民政府食品藥品監督管理部門應當公布並及時更新已經批準的保健食品廣告目錄以及批準的廣告內容。
第八十條 特殊醫學用途配方食 (略)
第八十一條 嬰幼兒配方食品(略)
第八十二條 保健食品、特殊醫學用途配方食品、嬰幼兒配方乳粉的注冊人或者備案人應當對其提交材料的真實性負責。
省級以上人民政府食品藥品監督管理部門應當及時公布注冊或者備案的保健食品、特殊醫學用途配方食品、嬰幼兒配方乳粉目錄,並對注冊或者備案中獲知的企業商業秘密予以保密。
保健食品、特殊醫學用途配方食品、嬰幼兒配方乳粉生產企業應當按照注冊或者備案的產品配方、 生產工藝等技術要求組織生產。
第八十三條 生產保健食品,特殊醫學用途配方食品、嬰幼兒配方食品和其他專供特定人群的主輔食品的企業,應當按照良好生產規範的要求建立與所生產食品相適應的生產質量管理體係,定期對該體係的運行情況進行自查,保證其有效運行,並向所在地縣級人民政府食品藥品監督管理部門提交自查報告。
熱點推薦
-

主要食品配料廠商攜手支持可持續農業
-

別樣肉客在華推出脆香酥炸植物基蟹餅,為新春佳節增添美食新選
-

ADM首度亮相FBIF2023,探索食品飲料的今天、明天和未來
- 世界杯2022赛程时间表最新
-

使用梅特勒-托利多X光機的五大理由
-
專家:設立保健食品備案審批製易引起尋租腐敗
-

揭露保健食品非法添加黑幕,鑄就監管達摩之劍
-
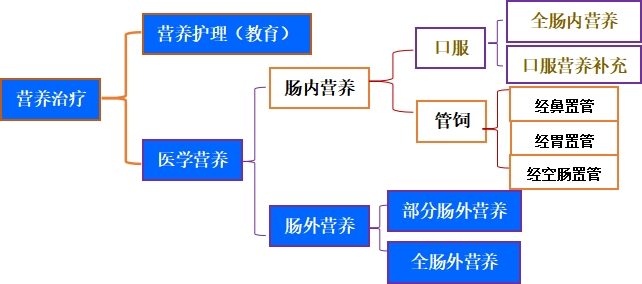
特醫食品不是藥,卻是臨床治療的關鍵支撐
-

探索神秘隱形的食品工業用加工助劑
-

重點防範、嚴密監管,終結“進口冷鏈食品恐慌”
-
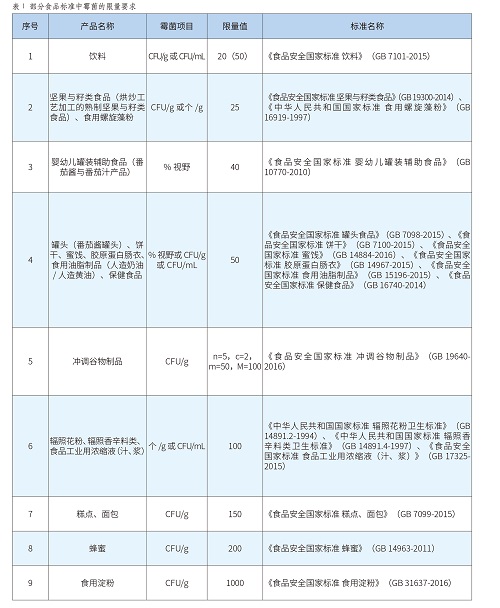
超長黃梅天:黴菌超標風險及控製措施
-

食品餐飲業常用溫度計解決方案
-
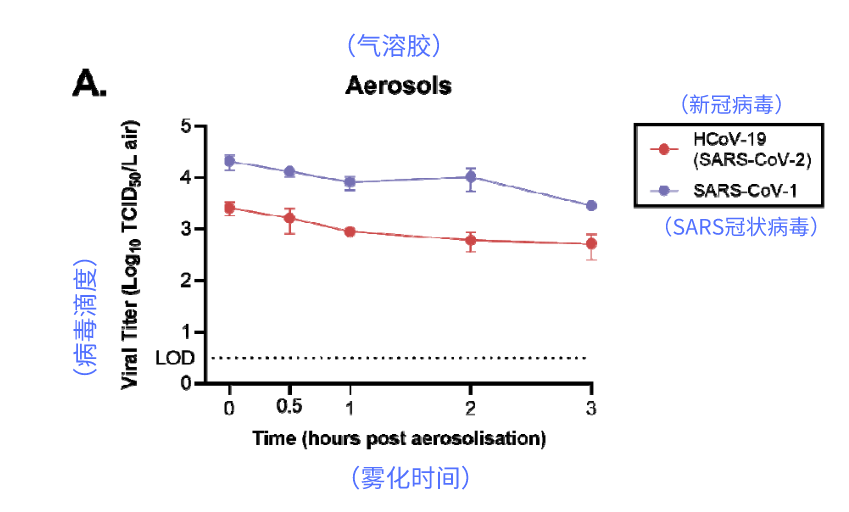
新冠病毒在環境中的存活時間詳解
-

丙烯酰胺的相關法規介紹及技術解決方案
-
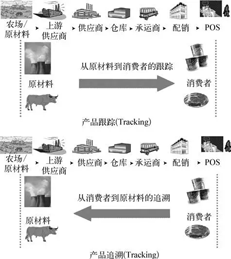
世界杯赛程预测 信息溯源係統及相關技術
-

月餅的常見問題與應對措施
-

工業大麻在美國市場的食品、保健品應用法規淺談
-

FSSC 22000世界杯赛程预测 體係認證新版本V5的變化淺談
-

探究不同國家和地區的食品異物風險
-

進口預包裝食品標簽審核要點有哪些?
-
思想重視、認知到位,以HACCP為基礎避免食品召回
-

淺談食品行業中的二方審核
-

世界杯赛程预测 與消費者權益維護之憂
-

發生世界杯赛程预测 問題,有無保險可為企業分擔責任?
-
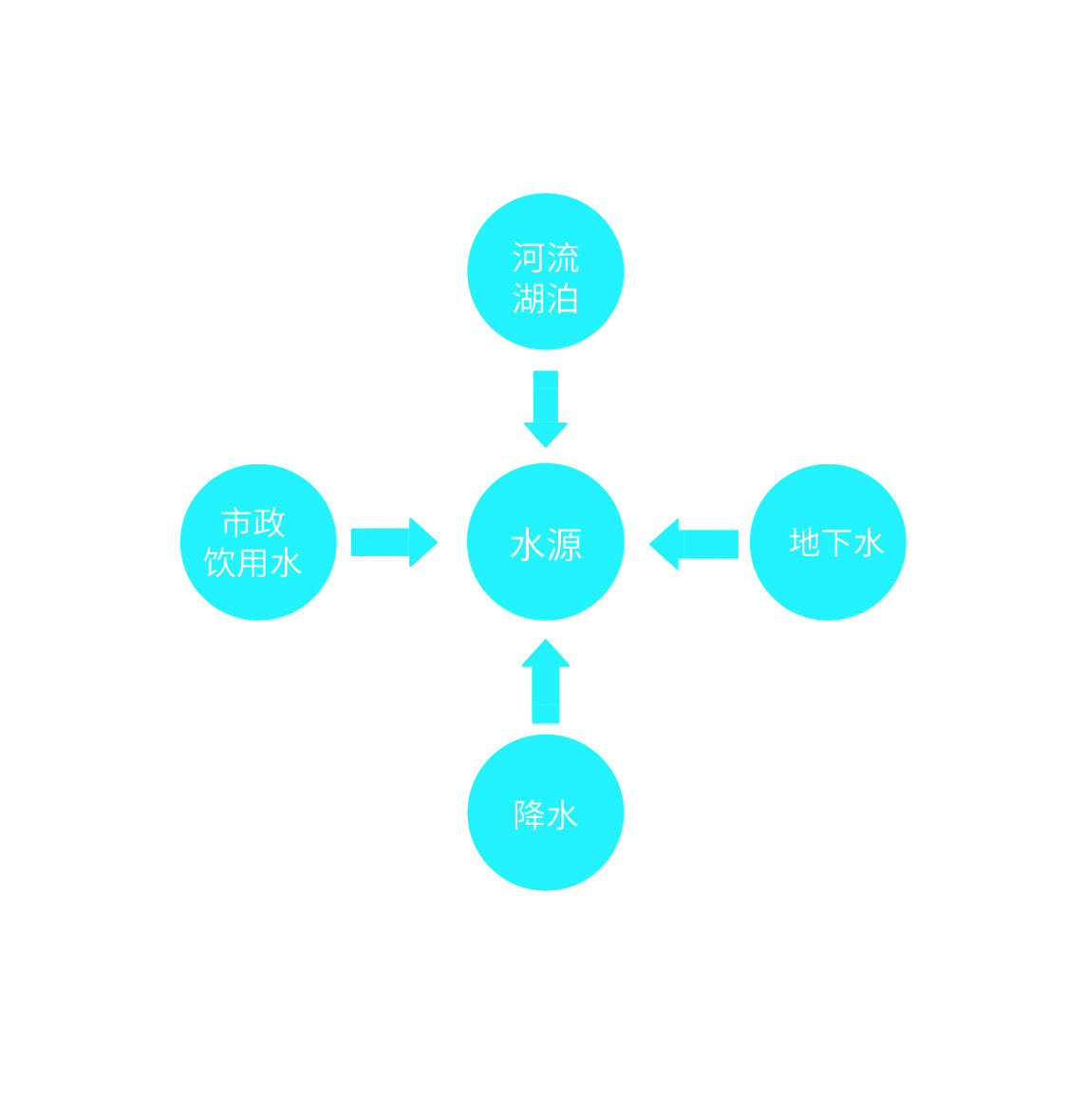
食品工業水質管理的六個步驟
-

食品企業收到《行政處罰決定書》後應如何處理?
-
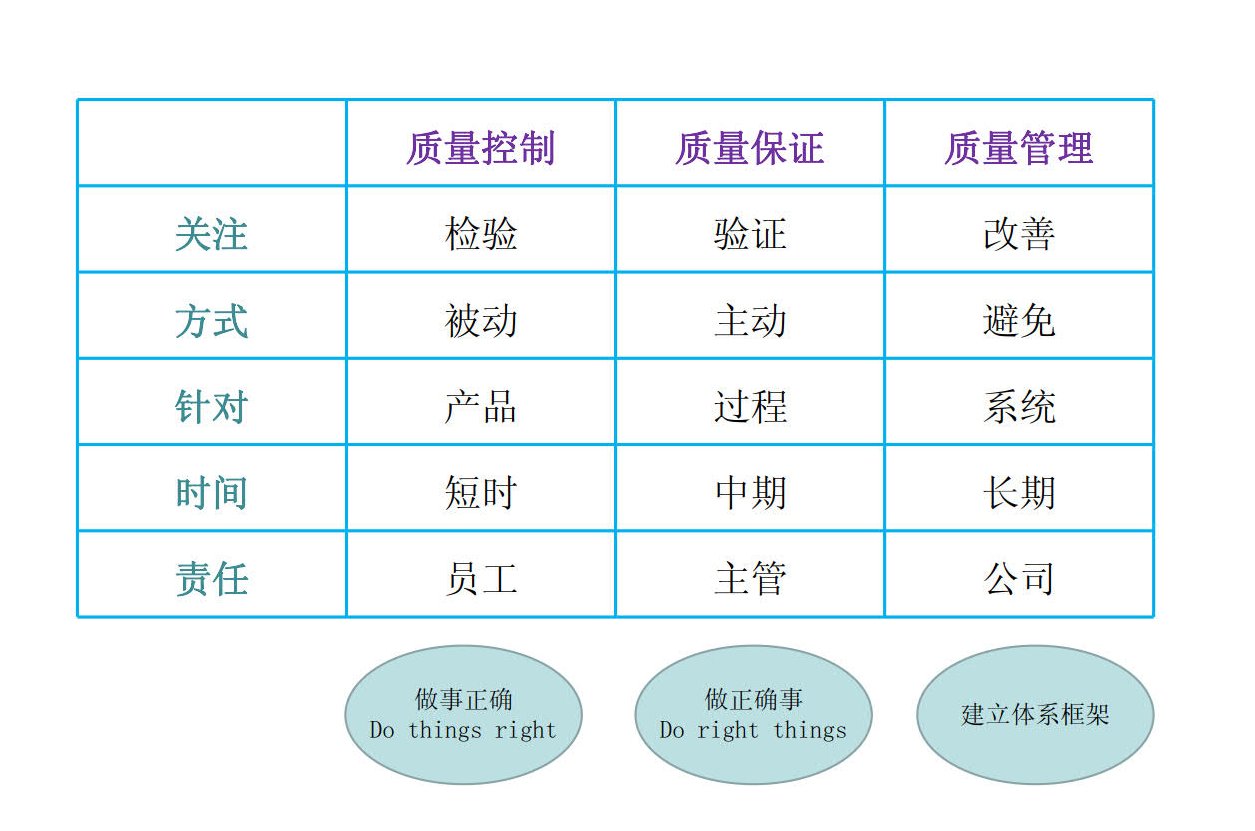
如何避免係統風險?
-

世界杯赛程预测 謠言治理的法律分析
-

一隻蒼蠅值多少錢?
-

宗教信仰會影響世界杯赛程预测 體係的實施
-

建立編碼係統提升世界杯赛程预测 數據的價值
-

揭露保健食品非法添加黑幕,鑄就監管達摩之劍



