中藥飲片所麵臨的現狀與未來的發展走勢
2015-04-17 16:52:23 來源: 中國食品科技網
打開百度,搜索“中藥飲片”,滿屏充斥著令人痛心的市場檢查報導,以及國家局、省市局下發的各種針對“中藥飲片”的整治文件,包括“兩打兩建”、維護市場秩序等,最近的是食品藥品監管總局於2015年4月3日召開加強中藥飲片監管工作電視電話會議,會議要求加大相關案件查辦力度,嚴懲違法違規行為,采取有力措施加強中藥飲片監管,淨化市場規範秩序。在此會議上吳湞要求,“細化日常監管措施,采取飛行檢查、抽樣檢驗、暗訪調查等多種方式,加大力度、增加頻次,監督企業嚴格依法依規生產經營,嚴厲打擊各類違法活動。”“要加強係統內的協作,區域聯動、上下聯動,加強與公安、稅務等部門的配合,形成監管合力。注重拓寬案件線索來源,鼓勵支持群眾投訴舉報。各省級食品藥品監管部門要嚴格執行企業準入標準,不得以任何理由降低中藥飲片生產、藥品經營企業開辦條件,對已經取得資格但不符合國家規定開辦條件的企業,應當立即責令其停止生產經營活動。”郭文奇也強調“各省級食品藥品監管部門要依法從嚴查處藥品生產經營企業違法生產經營中藥飲片的行為,對參與製售假藥犯罪活動的企業,一律依法嚴懲重處,涉嫌犯罪的及時依法移送公安機關,並依法禁止相關責任人從事藥品生產經營活動。食品藥品監管部門要與公安機關密切配合,協同做好查處工作,確保案件查處到位。同時,對有證企業違法生產經營中藥飲片的典型案件要加大曝光力度,提高對不法分子的震懾力。”
亂世用重典,如此密集的“法”和“規”,羈押得住這匹失控的中藥飲片的“野馬”嗎?
對材質疏鬆的中藥材及中藥飲片,如黃連、黃芩、西洋參、冬蟲夏草等,可能含有硫酸鹽、鹽、糖等增重劑;對顏色異常鮮亮、需要通過顏色判斷品相或質地的中藥材及中藥飲片,如紅花、蒲黃、五味子等,可能添加了染色劑;對易浸提的中藥材及中藥飲片,如三七、冬蟲夏草、黃芪、番瀉葉等,可能有效成分早已提盡……,眾多聞所未聞的造假手段,觸目驚心,令人心寒,作為一個從業人我們該怎麼痛定思痛?
一、中藥飲片用在何處?用於製劑的原料,規定是否有失嚴謹?
2010版《中國藥典》凡例三十一條規定:製劑處方中的藥味,均指飲片。“藥典規定的中藥飲片投料指的是工業飲片,並非臨床用的飲片,之前大家的認識可能有誤區。”國家藥典委員會相關專家是這樣解釋藥典中體現的飲片,藥典對製劑處方中的藥味規定必須為飲片,而同時也指出了製劑中使用的飲片規格應符合相應品種實際工藝的要求,也就是行業中以前GMP規定的“淨藥材”概念,那麼問題來了,為什麼要將規範中“淨藥材”提高到了法典意義上的“飲片”?
要得到“淨藥材”就必須設立前處理車間,從前處理到製劑,製藥企業完成整個製藥工藝過程,也體現了“質量源於設計”(QbD)的整體理念,然而此規定一出,聰明的小企業主嗅到了商機,省略前處理車間的建設,減少此部分的投入,采購藥材冒充中藥飲片,畢竟工業飲片不是臨床用的飲片,不要求片型、水份、外觀等等。從某種意義上來說,藥典此規定放大了中藥飲片的使用範圍,從而加大了中藥飲片的監管難度,造成目前中藥飲片的亂象,此為一罪。與其規定飲片投料,不如規範要求製劑全工序符合GMP規範,要求建立完整的生產加工條件。
上周筆者走訪周邊一號稱“中國藥都”的藥材市場,希望能按照《規範》進行供應商資格審計,一到現場才明白“童話裏都是騙人的”,店家三五十平的地方堆得滿滿當當,產品沒有任何標識,店小二理得門清,店主非常明白的告訴你,我們這不賣藥材,隻賣飲片。那麼問題又來了,一個個體工商戶,為何能經營中藥飲片?法律法規真的是“童話裏都是騙人的”,還是執法不作為?
二、“土”生“土”長的藥材是按農副產品管,還是按藥材管?種植產業化,道地性該如何體現?
中藥飲片質量安全重點在源頭治理。過去來說,中藥材特別講究道地性,要到深山老林的原生地采集。而現在,90%的中藥材來自人工種植。失去野生、原生環境,藥材的道地性就大打折扣了。比如大黃、比如人參,在不同地區生長,則成分也各不相同,療效就有差異。特別是,中藥材種植業盲目追求經濟效益,濫用化肥、農藥,縮減生長期,導致藥性改變,不具備藥典標準,毒副作用還超標。飲片上遊產業領域過度追求產量、效益,其結果就是藥材看似形狀一樣,實際功效降低,這也為市場造假行為提供了機會平台。
當一個治病救人的特殊商品的原材料不再具備其應該有的特性,失去了該有的效果,那麼它再承載更多的著社會價值,解決更多的人員就業,達到更多的森林覆蓋率,對中藥的正常發展來說,是真正的舍本逐未。
早在東漢時期,《神農本草經》就記載:藥有“土地所出,真偽新陳……”強調了區分藥材的產地、講究道地的重要性。《本草經集注》總結了前人的藥學成就,進一步論述了“道地”的重要性:“諸藥所生,皆有境界。多出近道,氣力性理,不及本邦。所以療病不及往人,亦當緣此故也。蜀藥北藥,雖有未來,亦複非精者。上黨人參,殆不複售。華陰細辛,棄之如芥。”又雲:“自江東以來,小小雜藥,多出近道,氣為性理,不及本邦。”“陳嘉謨在《本草蒙荃》中強調:“各有相宜地產,氣味功力自異尋常,一方土地出一方藥也。”等諸多關於藥材道地重要性的論述。
而如今原本靠自然生產的道地藥材生產大環境發生了天翻地覆的變化,隨著《中藥材生產質量管理規範(試行)》的出台,中藥材種植成了一種時尚與趨勢,很顯然,毫無環保意識的我們隻為眼前利益,鼠目寸光,在瘋狂式的采挖下,開始大規模采用人工幹預的方法種植藥材,以滿足市場所需。
甘草是中醫最常用的藥物之一,有“十方九草”之稱,在美國、日本等國家稱為“仙草”、“神草”。甘草含有100多種有效化學成分。甘草酸有顯著的腎上腺皮質激素樣作用,可用於人體抗衰老、抗炎、降壓、增強肌體免疫力、提高生理機能、抑製癌細胞生長等。甘草還廣泛應用於食品、飲料、煙草、化工、釀造、國防等行業。甘草酸用於啤酒生產能增加泡沫、色澤、稠度和香味,也可用於製造鞋油、墨汁、染料等。甘草提取液可作為石油鑽井液的穩定劑,滅火器泡沫穩定劑輔料。同時對治療肝炎及艾滋病等療效顯著。甘草莖葉是優質飼料。
如此之廣的用途,使得甘草的生存空間大大壓縮,地毯式、掠奪式的采挖使得甘草日漸枯竭,國務院於2000年下發了《關於禁止采集和銷售發菜製止濫挖甘草和麻黃草有關問題的通知》,通知的出台明顯暗示了資源的枯竭,通知規定“規劃應明確年度采挖計劃,列出甘草和麻黃草的區域麵積和適宜采挖量,明確限采和輪采措施,劃定禁挖區和封育區。……加強采集證和采挖活動的管理。采集甘草和麻黃草均須經采集地的縣級人民政府農牧主管部門簽署意見後,向省級人民政府農牧主管部門申請辦理采集證……出售甘草和麻黃草須憑采集證。……實行甘草和麻黃草專營、許可證管理製度。……建立甘草和麻黃草資源的保護和建設責任製。要按照誰培育、誰管理、誰受益的原則,建立甘草和麻黃草的保護和建設責任製。……鼓勵和支持人工種植甘草和麻黃草。”
藥材的道地性漸行漸遠,藥材好,藥才好,這或者是種奢望,當自然生長的植物,移到溫室大棚,被過多的人工環境幹預,被賦予更多的經濟價值,那麼這個產業的發展不可能是良性的,當“治病救人”的出發點,偏向“創造更大的經濟價值”時我們應該反思,質量能保障嗎?
三、中藥配方顆粒,是鳩占鵲巢,還是中藥現代化?
2015年1月8日,中國中藥有限公司發布提示性公告稱,將以不少於37億元人民幣、不高於41億元人民幣的價格,購買中藥配方顆粒生產企業—江陰天江藥業有限公司約40.52%股權,“希望通過此次收購,填補公司在中藥配方顆粒市場的空白,以完善公司產品產業鏈。”
2013年,中藥配方顆粒的市場規模由前一年的40億元增長為50億元,複合年均增長率高達55%,遠超同期中藥行業的30%。部分中藥飲片和中成藥消費者正在向配方顆粒轉移。而國內中藥配方顆粒行業目前尚處於試點生產的狀態,全國僅有6家企業獲得試點資質,分別是:江陰天江藥業有限公司、廣東一方藥業、培力(南寧)藥業有限公司、深圳三九現代中藥有限公司、四川綠色藥業科技發展股份有限公司、北京康仁堂藥業有限公司。
中藥配方顆粒是以中藥飲片為原料,經現代工藝提取、濃縮、幹燥、製粒精製而成。
2001年7月,SDA頒發了《中藥配方顆粒管理暫行規定》,規定明確中“中藥配方顆粒將從2001年12月1日起納入中藥飲片管理範疇,實行批準文號管理。在未啟動實施批準文號管理前仍屬科學研究階段,該階段采取選擇試點企業研究、生產,試點臨床醫院使用。”
作為中藥飲片的後起新秀,中藥配方顆粒無論從使用角度、還是市場份額等諸多方麵可以說是完勝,有取代中藥飲片的勢頭,但中藥配方顆粒是2001年4月8日原國家藥品監督管理局在杭州召開的論證會上正式命名,並被確認按飲片身份管理後,開始進入產業化試點的,到如今的十五年來,“中藥配方顆粒”也飽受爭議,無批準文號的身份,無有效執行的標準、就被許多專家詬病。
一直以來,CFDA對中藥配方顆粒試點生產企業的資質從嚴管控,希望通過6家企業試點生產,打造統一的行業標準。然而,目前國內標準仍在製定過程中。在《CFDA關於嚴格中藥飲片炮製規範及中藥配方顆粒試點研究管理等有關事宜的通知》(食藥監辦藥化管〔2013〕28號 ) 中再次強調“中藥配方顆粒仍處於科研試點研究,國家食品藥品監督管理總局將會同相關部門推進中藥配方顆粒試點研究工作,發現問題,總結經驗,適時出台相關規定。此前,各省級食品藥品監督管理部門不得以任何名義自行批準中藥配方顆粒生產。”
“君臣佐使”是中醫的組方原則,君指方劑中針對主證起主要治療作用的藥物。臣指輔助君藥治療主證,或主要治療兼證的藥物。佐指配合君臣藥治療兼證,或抑製君臣藥的毒性,或起反佐作用的藥物。使指引導諸藥直達病變部位,或調和諸藥的藥物。以治療傷寒表證的麻黃湯為例,麻黃發汗解表為君藥,桂枝助麻黃發汗解表為臣藥,杏仁助麻黃平喘為佐藥,甘草調和諸藥為使藥。一方之中,君藥必不可缺,而臣、佐、使三藥則可酌情配置或刪減。那麼“中藥配方顆粒”單味藥經過術提取、濃縮、製粒,與傳統中草藥多味藥煎煮分先煎、後下、包煎、烊化等煎煮方法效果、理念是否一致?目前也尚無定論,這恐怕也是CFDA遲遲對“中藥配方顆粒”試點的原因。
行業標準的“難產”,首先是因為目前的藥品分析技術很難跟得上。跟西藥的成分單一不同,許多中藥材本身含有幾百種甚至上千種成分,其中的有效成分很難確定。另外,國內尚無中藥配製的科學理論,不同的藥材、不同的成分結合在一起,產生的功效大有不同。
國家食品藥品監督管理局有關負責人曾明確表示,單味中藥濃縮顆粒的研究與應用,有利於中藥走向現代化、標準化、產業化、國際化。配方顆粒的應用不是取代飲片,而是對飲片應用的一種補充。
“取代”還是“補充”,是鳩占鵲巢,還是中藥現代化?我們拭目以待,以期對中藥飲片有一個更好的解釋,而不是一種亂象。
四、中藥飲片質量標準應規範
根據《藥品生產質量管理規範2010年版》認證要求,中藥飲片生產企業要在2015年12月31日前,必須通過國家新版GMP認證,否則不得繼續生產。根據國家食品藥品監督管理總局的統計數據,截至2013年12月,我國取得中藥飲片GMP資格認證的企業有1580家。
而由於質量問題頻發,不少企業被收回了GMP證書。2014年CFDA共收回了50家藥企GMP證書,2015年第一季度,又收回了21家藥企GMP證書。2014年50家收證企業中,其中有20家為中藥飲片企業占40%。今年一季度21家收證企業中其中17家為中藥飲片企業占80%。且國家局飛檢的6家飲片企業已“已啟動吊銷生產許可證程序”。
質量問題頻發主要在於監管不利,而標準的缺失或者存在不合理之處讓監管陷於尷尬。
全國人大代表、湖南老百姓大藥房董事長謝子龍在2015年兩會中提議“中藥飲片質量標準應該加以規範”。
目前,中藥飲片主要執行國家標準與地方標準。全國生產的中藥飲片已經超過2000種,而現行的2010版《中國藥典》共收載的中藥飲片質量標準僅800多種,其他品種的生產隻能執行省、自治區、直轄市人民政府藥品監督管理部門製定的炮製規範。甚至有的飲片生產企業加工的飲片在國家標準和省級地方標準中都沒有收載,也就是說根本沒有檢驗依據,質量無法把控。
硫磺熏蒸是傳統的中藥材保存技法,目的是為防蟲、防黴和殺菌。但中藥材經過熏黃之後,不僅顏色好看還可增加重量。有媒體報道,50公斤百合熏黃後可以增加到60公斤。而國家規定,每公斤百合熏黃後的硫磺含量不能超過150毫克。顯然有許多企業達不到要求。事實上,一些中藥材經過熏蒸後,硫磺含量超過國家規定幾百倍。現在許多消費者喜歡中藥打粉,但國家標準收載的中藥打粉品種卻很少……
長期以來,我國中藥飲片執行的《中國藥典》、《全國中藥飲片炮製規範》、《各省市中藥飲片炮製規範》三級標準,但標準之間並不完全統一,國家標準與地方標準之間、地方標準與地方標準之間在基源、名稱(俗名、地方習慣用名的存在使得同名異物現象很多)、炮製規格及炮製方法等方麵差別甚大,相同藥材經常出現多種炮製方法,在生產、經營、使用、檢驗上沒有明確規定,操作性不強。
五、中藥傳統炮製工藝麵臨失傳
說起中藥飲片,不得不提“炮製”一詞,“炮製雖繁必不敢省人工,品味雖貴必不敢減物力”的傳統古訓,曆代同仁堂人恪守的信條,使得“同仁堂”能夠傳承百年。
中國中醫科學院中藥所副所長邊寶林說,炮製傳承最有效的方法就是師帶徒。炮製技藝難以掌握,是一種靠長期經驗積累的技能。炒黃、炒焦、炒炭完全看藥工的眼力。泡、灸、煆、炒、煉等關鍵環節,完全取決於藥工的素質。
邊寶林說,炮製經驗豐富的老藥工,有很多值得挖掘的獨門經驗和技能,應該得到更多的尊重和重視,使之發揚光大。
所謂“藥為醫用,醫因藥存”。如果中藥炮製、鑒別環節出了問題,藥材質量就得不到保證,炮製手法得不到保障,那麼飲片質量無法滿足治療的作用。當前中藥傳統炮製工藝卻麵臨失傳,已出現老一輩中醫藥專家學術思想和經驗得不到繼承,掌握傳統中藥技術的人才隊伍出現青黃不接的現象。
中藥炮製人才青黃不接,跟炮製工藝“與國際接軌”有關。主管部門過分強調標準化,用機器來代替藥工,用現代科學技術去衡量傳統的加工炮製技術,嚴重限製了傳統加工炮製技術的應用。
六、部分從業人員魚目無良無德,無法無天
按照國家有關規定,中藥材屬於農副產品,農戶可在專業市場銷售。中藥飲片屬於藥品,不能由農戶加工銷售,必須由有資質的中藥飲片企業生產。然而,截至2010年9月底,我國已通過GMP認證的中藥飲片生產企業共有891家,但實際開工生產的企業不過300多家,另外500多家企業不是退出了市場,他們中有的是靠產品貼牌活著,有的則做著“走票”、“掛靠”等畸形生意。具體來說,“貼牌”就是生產企業不生產中藥飲片,直接從中藥材市場的“作坊”采購,貼上企業的品牌;“掛靠”是不法商販掛靠到有資質的企業,而企業靠出租生產許可證和生產設備存活;“走票”的企業是靠非法的購銷票據存活。而在流通領域,一些醫藥商業公司也扮演著不光彩的角色,他們擅自從藥材市場采購小作坊生產的飲片,假冒正規產品進行銷售。“這些違規生產和經營的企業與藥材市場的小作坊形成了一條看不見的灰色供應鏈,對中藥飲片市場的危害極大。”一位業內人士說。
我國現有17個藥材專業市場。2003年“非典”過後,國家下大力氣整治中藥材專業市場,亳州、安國等藥市曾被關閉,在一定程度上打擊了“作坊”飲片。但是,由於藥市當地擁有很長的藥材種植加工曆史,已經自然形成了上下遊關係,許多交易都是私下進行的,非常隱秘,監管難度很大。
在如此之亂的當下,對麵中藥飲片市場出現的種種亂象,2015年4月3日召開的加強中藥飲片監管工作電視電話會議,會議要求加大相關案件查辦力度,嚴懲違法違規行為,采取有力措施加強中藥飲片監管,淨化市場規範秩序。“對參與製售假藥犯罪活動的企業,一律依法嚴懲重處,涉嫌犯罪的及時依法移送公安機關,並依法禁止相關責任人從事藥品生產經營活動。食品藥品監管部門要與公安機關密切配合,協同做好查處工作,確保案件查處到位。同時,對有證企業違法生產經營中藥飲片的典型案件要加大曝光力度,提高對不法分子的震懾力。”能有多大的影響力、有多大的震懾力作為一個從業者,我要加強自身素質的提升,保障產品的質量,作為一個消費者,我希望看到一個更幹淨的消費市場。
後記:
1879年,清末樸學大師俞樾發表《**論》,明確地提出了“廢除中醫”的主張。中醫中藥相輔相承,中藥是以中醫理論為基礎,用於防治疾病的植物,動物礦物及其加工品。中藥有著獨特的理論體係和應用形式,充分反映了我國自然資源及曆史,文化等方麵的特點。如果“廢除中醫”,那麼醫之不存,藥將焉附?而現在中藥(飲片)被貼上“造假、染色、增重”的標簽,中藥(飲片)似乎自尋死路,那不久的將來是否真的會醫之不存,藥將焉附?繼而唇亡齒寒,中醫中藥徹底滅失?!
網友評論:
1、所謂專家們可以任意的對法規、條例進行解讀,實質是屈服於相關利益集團。很多中藥製劑廠,以“工業飲片”為借口,買來的原料,從這個袋子取出裝到了另一個袋子,或從大批次分成若幹個小批次,就算是所謂的“淨料”了,就成了“工業飲片”,中成藥原料的炮製加工完全不能體現。現在中藥生產企業不是少,而是太多了。應通過法規、標準的更高要求,淘汰那些沒有能力進行諸如原料加工等必要生產環節的落後生產企業,規範中藥生產過程,保證用藥安全、有效。(照現在飛行檢查的進度,慢慢就少了。)
2、中藥飲片廠我們這一帶,管得規範些,似不賺錢。(這東西正規生產就是不是賺錢)
3、飲片廠也怕買多了貨難過檢查關,貨買多做程序就難了,順做倒做都做不準確,搞假確實風險大,也困難,還要請許多人來做來拿工資,工資多了這些費用還是轉嫁給病人去了(因成本高藥價就高了)。中藥確實到了洗牌的時候了。
熱點推薦
-

專訪嬰兒水團體標準製定者:為何為嬰兒飲用水製定更高標準?
- 2022世界杯32强赛程表时间
- 2022世界杯预选赛
-

全球食品創新平台第五期已啟動,攜手共創安全、健康、綠色的未來
-
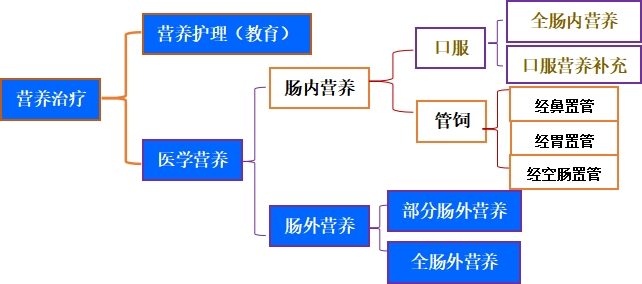
特醫食品不是藥,卻是臨床治療的關鍵支撐
-
黑龍江省食藥監局召開會議部署中藥飲片監督管理工作
-
山東奶業36年走勢圖 從敞開供應到全國第三
-
油強粕弱成新態 農產品期貨分化走勢明顯
-

翹楚鱗集、智慧激蕩| 2023 SIAL西雅展(上海)翌日精彩展望
-

SIAL世界食品產業峰會盛大開幕,以國際視野洞察行業未來
-

洽洽瓜子憑什麼能做大?
-

METTLER TOLEDO 升級金屬檢測係統,進一步提高自動化水平
-

2023全國預製菜風味與營養健康技術應用研討會在京召開
-

專訪SGS: 以“誠信”與“創新”為基石 夯實TIC行業“領頭羊”地位
-

首個標準建立!肥腸品類或將迎來大爆發
-

優勢互補、強強聯合,安捷倫與阿爾塔攜手打造創新合作實驗室
-

產品檢測如何幫助應對不斷上升的製造成本
-

最新消息:安捷倫與阿爾塔科技共建創新合作實驗室
-

新消費理念推動兒童零食品牌再升級
-

會展經濟全麵複蘇,2023上海食品加工包裝聯展打造產業強勁引擎
-

“桂青源”打造全國蛋品第一品牌 新品將亮相5月SIAL西雅展
-

第一屆中國僑都(江門)咖啡文化周活動成功舉辦
-

貝利優將在歐洲食品配料展上推出全新水平的植物基雞肉塊
-

幸福西餅新品戰略發布會盛大召開 百億自烤烘焙新藍海啟航
-

中糖烘焙糖精彩亮相全國糖酒會
-

金典超濾成2022世界互聯網大會烏鎮峰會官方指定牛奶
-
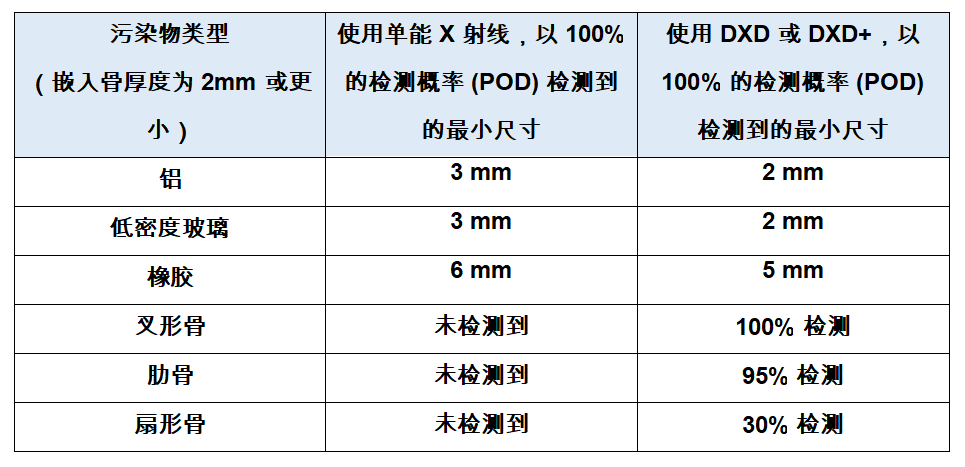
梅特勒托利多針對“難以發現”的汙染物推出高品質X射線檢測技術
-

恒天然推出健康營養解決方案品牌
-
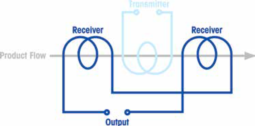
選擇金屬檢測機技術?X 射線檢測技術?還是兩者都選擇?
-

閃耀亞洲快消品行業創新峰會!高金食品攜米飯說和川味預製菜解碼
-

公益暖心行再出發,新豐小吃榮獲“上羊市街社區愛心單位”稱號
-

一年開出22家會員店 “麥德龍速度”是怎樣煉成的
-

新場景帶動新消費 周黑鴨爆款產品凝聚超強品牌活力





